题目内容
某标示为5%的过氧化氢溶液已放置了一段时间,为了检测过氧化氢的质量分数是否仍为5%,取该溶液20g使其在MnO2作用下发生反应.每隔一段时间作一次记录,实验过程记录如下:| 反应过程记录 (按时间顺序) | 1 | 2 | 3 | 4 | 5 |
| 产生O2的质量/g | 0.12 | 0.25 | 0.36 | 0.40 | 0.40 |
【答案】分析:可以根据生成氧气的质量,通过化学方程式求出过氧化氢的质量,从而进一步求出过氧化氢溶液的质量分数.
解答:解:设20g过氧化氢溶液含有的过氧化氢的质量为X,
由表中数据可知,第四次和第五次记录的结果相同,说明第四次时,过氧化氢已经完全分解,生成氧气的质量是0.40g,
2H2O2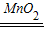 2H2O+O2↑
2H2O+O2↑
68 32
X 0.40g
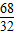 =
=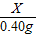
X=0.85g,
过氧化氢溶液的质量分数为: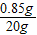 ×100%=4.25%,
×100%=4.25%,
通过计算可知该溶液的溶质质量分数变小了.
点评:本题比较容易,关键是能够通过表中信息判断出何时完全反应,并且知道完全反应后生成氧气的质量.
解答:解:设20g过氧化氢溶液含有的过氧化氢的质量为X,
由表中数据可知,第四次和第五次记录的结果相同,说明第四次时,过氧化氢已经完全分解,生成氧气的质量是0.40g,
2H2O2
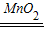 2H2O+O2↑
2H2O+O2↑68 32
X 0.40g
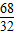 =
=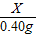
X=0.85g,
过氧化氢溶液的质量分数为:
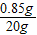 ×100%=4.25%,
×100%=4.25%,通过计算可知该溶液的溶质质量分数变小了.
点评:本题比较容易,关键是能够通过表中信息判断出何时完全反应,并且知道完全反应后生成氧气的质量.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
某标示为5%的过氧化氢溶液已放置了一段时间,为了检测过氧化氢的质量分数是否仍为5%,取该溶液20g使其在MnO2作用下发生反应.每隔一段时间作一次记录,实验过程记录如下:
| 反应过程记录 (按时间顺序) | 1 | 2 | 3 | 4 | 5 |
| 产生O2的质量/g | 0.12 | 0.25 | 0.36 | 0.40 | 0.40 |