题目内容
【题目】氯化钙(CaCl2)可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含有少量Al2O3、Fe2O3、SiO2等杂质)制备氯化钙的主要流程如下:
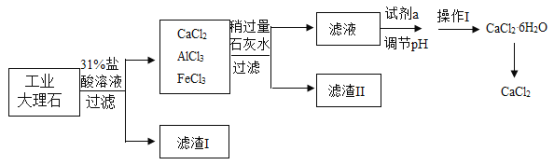
请回答下列问题:
(1)配制31%的稀盐酸730 g,需要36.5%的浓盐酸______g。
(2)酸溶时碳酸钙参与反应的化学方程式为_______。
(3)滤渣I的成分为____,滤渣II中含有Al(OH)3和______。
(4)过滤使用到的玻璃仪器有____。操作I采用的方法是:蒸发浓缩、_____、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应的化学方程式为_____。
【答案】620 CaCO3+2HCl=CaCl2+CO2↑+H2O SiO2 Fe(OH)3 烧杯、玻璃棒、漏斗 冷却结晶 Ca(OH)2+2HCl=CaCl2+2H2O
【解析】
(1)配制31%的稀盐酸730g,需要36.5%的浓盐酸质量为31%×730g÷36.5%=620g。
(2)酸溶时,碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O。
(3)二氧化硅和稀盐酸不发生反应,滤渣I的成分为SiO2,氯化铝和氯化铁和氢氧化钙反应生成氢氧化铝和氢氧化铁沉淀,滤渣II中含有Al(OH)3和Fe(OH)3。
(4)过滤使用到的玻璃仪器有烧杯、玻璃棒、漏斗;操作I采用的方法是:蒸发浓缩、冷却结晶、过滤。
(5)加入试剂a的目的是中和稍过量的石灰水,该反应是适量的稀盐酸和氢氧化钙反应生成氯化钙和水,化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目