题目内容
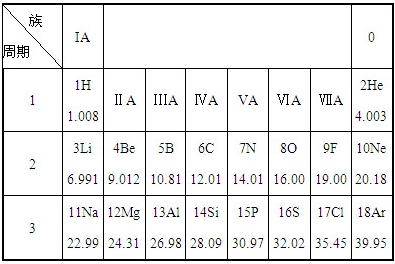
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字:
(2)查出碳的相对原子质量:
(3)表中不同种元素最本质的区别是
A.质子数不同;B.中子数不同;C.相对原子质量不同;D.电子数不同.
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期,近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为
(5)周期表中每一个横行叫做一个周期.第三周期开头元素和靠近尾部元素的原子结构示意图分别为
 ,它们的单质易发生如下图所示变化:
,它们的单质易发生如下图所示变化:
根据以上信息,可以得到的结论是
(2)从元素周期表中可查出碳的相对原子质量为12.01,16号元素的元素符号S,故答案为:12.01;S;
(3)不同种元素最本质的区别是质子数不同,故选A;
(4)在原子中,原子序数=质子数=核外电子数,第118号元素的核电荷数为118,故答案为:118;
(5)在原子中,质子数=核外电子数,在化学反应中,金属元素的原子比较容易失去最外层的电子,非金属元素的原子比较容易得到电子,得到稳定结构,故答案为:氯化钠是钠原子与氯原子通过电子的得失形成的.

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
族
周期 |
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 炭 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息:___________________________。
(2)请从上表中找出一种元素名称是错误的,更正为 .
(3)第3周期(横行)中属于金属元素的是 (填一种元素符号),其阳离子是 。
(4)在金属活泼性中,镁元素比铝元素活泼,请你从原子结构的观念进行解释 。
(5)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻, 其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水,该反应的化学方程式为 。
元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
|
|
I A |
II A |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(1)请从上表中查出关于硼元素的一条信息: 。
(2)第3周期中相对原子质量最大的金属元素的是 。
(3)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.C和Ne b.Be和Mg c.Al和Si d.F和Cl
(4)第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体和水,该反应的化学方程式为 。