题目内容
判断某瓶KNO3溶液是否饱和的正确做法是( )
| A、取样,加入少量KCl固体,观察能否继续溶解 | B、取样,加入少量KNO3固体,观察能否继续溶解 | C、取样,使其温度升高,观察是否有晶体析出 | D、取样,使其温度降低,观察是否有晶体析出 |
练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列关于溶液的说法正确的是( )
| A、均一、稳定的液体一定是溶液 | B、碘酒中的溶质是酒精 | C、用汽油洗去衣服上的油污是乳化现象 | D、相同温度,溶质相同的饱和溶液溶质的质量分数一定比不饱和溶液大 |
下列固体物质溶于水后,能使液体温度明显降低的是( )
| A、氯化钠 | B、硝酸铵 | C、生石灰 | D、氢氧化钠 |
下列物质加入一定量的水中,能使液体温度变低的是( )
| A、NH4NO3 | B、NaOH | C、CaO | D、NaCl |
20℃时,在三个各盛有100g水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各10g,充分溶解后,情况如下表所示( )
| 物质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 5 | 2 | 0 |
| A、所得溶液一定都是饱和溶液 |
| B、丙溶液一定是不饱和溶液 |
| C、丙溶液的溶质的质量分数最大 |
| D、20℃,时,甲的溶解度最大 |
下表为氢氧化钙在不同温度下的溶解度
室温下(20℃)下,将5.6g氯化钙投入到94.4g水中,充分搅拌,静置一段时间后,恢复到原来的温度(不计水分蒸发),参考上表,下列关于所得溶液的叙述中正确的是( )
| 温度/℃ | 8 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | Ca(OH)2 | 0.187 | 0.178 | 0.265 | 0.153 | 0.141 | 0.129 | 0.116 |
| A、溶质的质量是7.4g |
| B、溶液的质量是100g |
| C、溶液为饱和溶液 |
| D、溶质质量分数小于5.6% |
下列有关溶液的说法正确的是( )
| A、不饱和溶液转化为饱和溶液溶质的质量分数一定变大 | B、同种溶质的饱和溶液一定比它的不饱和溶液溶质的质量分数大 | C、饱和溶液转化为不饱和溶液溶液的质量一定增大 | D、饱和溶液恒温蒸发部分溶剂后溶质的质量分数一定不变 |
如图所示,给饱和澄清石灰水加热.以下叙述不正确的是( )


| A、溶液由澄清变浑浊 | B、溶液仍为饱和溶液 | C、溶液中溶质的质量分数减少 | D、Ca(OH)2的溶解度随温度的升高而增大 |
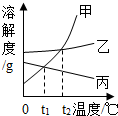 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法错误的是( )| A、t2℃时甲、乙两物质的溶解度相等 | B、温度大于t2℃时,甲、乙、丙三种固体物质溶解度的大小关系是甲>乙>丙 | C、当甲中混入少量乙时,可用冷却热饱和溶液的方法得到较纯净的甲 | D、t2℃时甲、丙两物质的饱和液降温到t1℃时,两者所得溶液的溶质质量的分数一定相等 |
