题目内容
【题目】某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分是 Fe2O3)炼铁的主要反应原理,他们设计的实验装置如图所示.
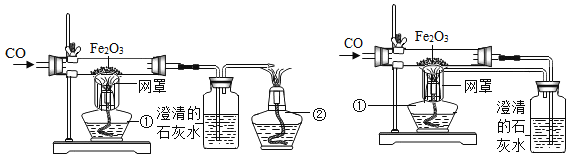
回答下列问题:
(1)写出用一氧化碳还原氧化铁的化学方程式__________________。
(2)实验时,在澄清石灰水中观察到的现象是_____________________。反应的化学方程式是________________________。
(3)图(乙)与左图相比,它的主要优点是_________________________。
【答案】Fe2O3+3CO高温2Fe+3CO2清的石灰水变浑浊CO2 + Ca(OH)2 == CaCO3 ↓+ H2O一氧化碳可回收利用
【解析】根据炼铁的原理可知,一氧化碳在高温的条件下还原氧化铁得到铁和二氧化碳,反应的化学方程式表示为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
反应生成的二氧化碳会与澄清石灰水反应生成碳酸钙沉淀和水,故观察到的现象是澄清的石灰水变浑浊,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
该实验中,由于要先通一氧化碳易排尽玻璃管中的空气,而一氧化碳有毒,排放到空气中会污染空气。图甲装置是直接点燃一氧化碳转化为二氧化碳,而图乙装置则先把混合物气体中的二氧化碳除去,再把未反应的一氧化碳通到前面反应装置的酒精灯处,利用了一氧化碳燃烧放出的热量。故图乙的优点是对一氧化碳进行了回收利用。

练习册系列答案
相关题目