题目内容
27、实验室中有一烧杯废液,可能由K2SO4、NaCl、NaOH、NaNO3、H2SO4、HNO3、FeCl3七种溶液中的几种溶液混合而成,安宁同学想探究其成分,进行如下实验:
(假设每步均恰好完全反应)
①观察混合溶液呈无色;
②取少量混合溶液,向其中加入适量的Ba(NO3)2溶液,过滤,得到白色沉淀A和滤液M;
③向滤液M中加入适量AgNO3溶液,过滤,得到白色沉淀B和滤液N;
④向滤液N中滴加几滴紫色石蕊试液,溶液呈红色.
请推断:
(1)A是
(2)原混合溶液的pH
(3)滤液M中含有的阴离子是
(4)原混合溶液中一定含有的溶质是
(假设每步均恰好完全反应)
①观察混合溶液呈无色;
②取少量混合溶液,向其中加入适量的Ba(NO3)2溶液,过滤,得到白色沉淀A和滤液M;
③向滤液M中加入适量AgNO3溶液,过滤,得到白色沉淀B和滤液N;
④向滤液N中滴加几滴紫色石蕊试液,溶液呈红色.
请推断:
(1)A是
BaSO4
,B是AgCl
(写化学式);(2)原混合溶液的pH
<
7(填“>““<”或“=“);(3)滤液M中含有的阴离子是
C1-和NO3-
;(4)原混合溶液中一定含有的溶质是
NaCl
(写化学式).分析:①混合溶液呈无色,废液中一定无氯化铁,因为含有铁离子的溶液为黄色;②加入适量的硝酸钡溶液,过滤,得到白色沉淀A为硫酸钡.K2SO4、H2SO4都可与Ba(NO3)2溶液生成白色沉淀.③适量AgNO3溶液,过滤,得到白色沉淀B为氯化银,④向滤液N中滴加几滴紫色石蕊试液,溶液呈红色,说明溶液为酸性.⑤指出:只能确定原溶液中有NaCl,其他无法确定.因为硝酸和硝酸钠有可能是反应生成的.
解答:解:实验室中有一烧杯废液,可能由K2SO4、NaCl、NaOH、NaNO3、H2SO4、HNO3、FeCl3七种溶液中的几种溶液混合而成,
(1)由分析知,①K2SO4、H2SO4都可与Ba(NO3)2溶液生成白色沉淀A为BaSO4;②适量AgNO3溶液,过滤,得到白色沉淀B为AgCl
(2)紫色石蕊试液呈红色,说明溶液为酸性.因为K2SO4、H2SO4都可与Ba(NO3)2溶液生成硝酸,所以原混合溶液的pH<7.
(3)既然能生成氯化银沉淀,所以滤液M中含有的阴离子是氯离子和硝酸根离子.
(4)白色沉淀A为硫酸钡,所以废液中可能含有硫酸钾或硫酸,同时可能有硝酸生成;AgNO3溶液和氯化钠生成氯化银和硝酸钠.
故原只能说可能含有硝酸和硝酸钠,所以原混合溶液中一定含有的溶质是:氯化钠.
故答为:(1)BaSO4,AgCl (2)<、(3)C1-和NO3-(或氯离子和硝酸根离子) (4)NaCl
(1)由分析知,①K2SO4、H2SO4都可与Ba(NO3)2溶液生成白色沉淀A为BaSO4;②适量AgNO3溶液,过滤,得到白色沉淀B为AgCl
(2)紫色石蕊试液呈红色,说明溶液为酸性.因为K2SO4、H2SO4都可与Ba(NO3)2溶液生成硝酸,所以原混合溶液的pH<7.
(3)既然能生成氯化银沉淀,所以滤液M中含有的阴离子是氯离子和硝酸根离子.
(4)白色沉淀A为硫酸钡,所以废液中可能含有硫酸钾或硫酸,同时可能有硝酸生成;AgNO3溶液和氯化钠生成氯化银和硝酸钠.
故原只能说可能含有硝酸和硝酸钠,所以原混合溶液中一定含有的溶质是:氯化钠.
故答为:(1)BaSO4,AgCl (2)<、(3)C1-和NO3-(或氯离子和硝酸根离子) (4)NaCl
点评:本题主要考查常见物质的鉴别和推断,了解溶液的酸碱度和PH值的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
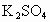 、NaCl、NaOH、
、NaCl、NaOH、 、
、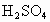 、
、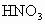 、
、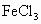 七种溶液中的几种溶液混合而成,安宁同学想探究其成分,进行如下实验:(假设每步均恰好完全反应)
七种溶液中的几种溶液混合而成,安宁同学想探究其成分,进行如下实验:(假设每步均恰好完全反应)
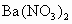 溶液,过滤,得到白色沉淀A和滤液M;
溶液,过滤,得到白色沉淀A和滤液M;
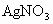 溶液,过滤,得到白色沉淀B和滤液N;
溶液,过滤,得到白色沉淀B和滤液N;