题目内容
核电荷数为1~18的x、y两元素,x元素原子的次外层电子数与最外层电子数的差等于5;y元素比x元素的原子多4个电子,则y与x可能形成的化合物是( )A.xy
B.xy2
C.xy3
D.x2y
【答案】分析:根据原子的每层电子数的关系来推断元素,然后利用最外层电子数来分析元素的化合价,最后利用化合价来判断生成的化合物.
解答:解:核电荷数为1~18的x、y两元素,
由x元素原子的次外层电子数与最外层电子数的差等于5,
若为2个电子层,则次外层电子数为2,最外层电子数为2+5=7,则质子数为2+7=9,即为F元素,因最外层电子数为7,则在化合物中元素的化合价为-1价,
若为3个电子层,则次外层电子数为8,最外层电子数为8-5=3,则质子数为2+8+3=13,即为铝元素,因最外层电子数为3,则在化合物中元素的化合价为+3价,
而y元素比x元素的原子多4个电子,
即x元素为F时,y元素的质子数为9+4=13,则y为Al元素,
由化合物中正负化合价的代数和为0,则可形成yx3,没有该选项;
当x元素为Al时,y元素的质子数为13+4=17,则y为Cl元素,其最外层电子数为7,在化合物中元素的化合价为-1价,
由化合物中正负化合价的代数和为0,则可形成xy3,
故选C.
点评:本题较难,学生应学会假设x元素的电子层,利用每层电子数的关系来推测符合条件的元素,即x元素的推断是解答本题的关键,并注意假设的前提是核电荷数为1~18的元素.
解答:解:核电荷数为1~18的x、y两元素,
由x元素原子的次外层电子数与最外层电子数的差等于5,
若为2个电子层,则次外层电子数为2,最外层电子数为2+5=7,则质子数为2+7=9,即为F元素,因最外层电子数为7,则在化合物中元素的化合价为-1价,
若为3个电子层,则次外层电子数为8,最外层电子数为8-5=3,则质子数为2+8+3=13,即为铝元素,因最外层电子数为3,则在化合物中元素的化合价为+3价,
而y元素比x元素的原子多4个电子,
即x元素为F时,y元素的质子数为9+4=13,则y为Al元素,
由化合物中正负化合价的代数和为0,则可形成yx3,没有该选项;
当x元素为Al时,y元素的质子数为13+4=17,则y为Cl元素,其最外层电子数为7,在化合物中元素的化合价为-1价,
由化合物中正负化合价的代数和为0,则可形成xy3,
故选C.
点评:本题较难,学生应学会假设x元素的电子层,利用每层电子数的关系来推测符合条件的元素,即x元素的推断是解答本题的关键,并注意假设的前提是核电荷数为1~18的元素.

练习册系列答案
相关题目
核电荷数为1~18的元素中,某微粒结构示意图为: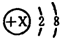 则该微粒( )
则该微粒( )
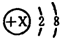 则该微粒( )
则该微粒( )| A、一定是阳离子 | B、一定是阴离子 | C、一定是氖原子 | D、无法确定 |

 ,则该离子带
,则该离子带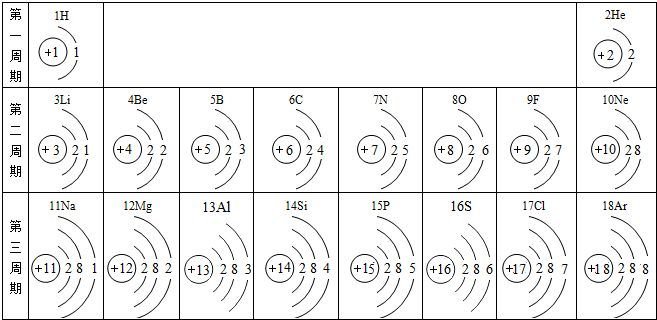 (1)在第二周期中,各原子结构的共同之处是
(1)在第二周期中,各原子结构的共同之处是