题目内容
兴趣小组同学做了以下探究实验:
(1)探究实验室中久置的氢氧化钠的成分.
【对固体猜想】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物.
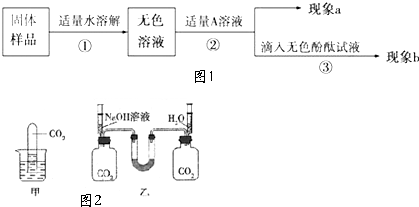
【实验和推断】见图1
i.若现象a为有气泡产生,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是 .
ii.若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为 (填化学式),该实验 (填“能”或“不能”)说明样品中有NaOH.
iii.若A是CaCl2溶液,当实验现象a为有 ,现象b为 ,则猜想Ⅱ成立.
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示) .
(2)验证氢氧化钠溶液能与二氧化碳反应.
做了下面两个实验.实验一:如图2甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况.
实验二:如图2乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况.请问:
i.实验乙中若观察到U形管左端的液面 (填“升高”或“降低”),则证明溶液中的氢氧化钠能与二氧化碳反应.
ii.与实验甲相比,同学们认为实验二更合理,因为 .
(1)探究实验室中久置的氢氧化钠的成分.
【对固体猜想】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物.

【实验和推断】见图1
i.若现象a为有气泡产生,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是
ii.若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为
iii.若A是CaCl2溶液,当实验现象a为有
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)
(2)验证氢氧化钠溶液能与二氧化碳反应.
做了下面两个实验.实验一:如图2甲,将一支充满二氧化碳的试管倒扣在盛有氢氧化钠溶液的烧杯中,观察试管中的液面变化情况.
实验二:如图2乙,向两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠溶液和蒸馏水,振荡后放在水平的桌面上,观察U形管(装有红墨水)两端液面的变化情况.请问:
i.实验乙中若观察到U形管左端的液面
ii.与实验甲相比,同学们认为实验二更合理,因为
分析:【实验和推断】根据氢氧化钠的性质进行分析,氢氧化钠露置在空气中易与二氧化碳反应生成碳酸钠而变质,反应的程度不同,则变质的程度不同;检验碳酸盐使用的是加酸化气的方法或加入含有可溶性钙离子、钡离子的方法,要证明含有氢氧化钠,则需要除去碳酸钠再进行检验,且加入的试剂与碳酸钠反应后不能生成显碱性的物质.
【反思】根据氢氧化钠与二氧化碳反应生成碳酸钠和水,则可书写化学方程式;
i.根据U型管两端的气压变化来分析、填空;
ii.验证性实验一般可采取排除其他物质的干扰进行实验,可此处无法排除水的干扰,那么只好做两组有蒸馏水存在的不同实验进行对比.
【反思】根据氢氧化钠与二氧化碳反应生成碳酸钠和水,则可书写化学方程式;
i.根据U型管两端的气压变化来分析、填空;
ii.验证性实验一般可采取排除其他物质的干扰进行实验,可此处无法排除水的干扰,那么只好做两组有蒸馏水存在的不同实验进行对比.
解答:解:【实验和推断】
i.氢氧化钠变质生成的是碳酸钠,如果加入A后产生气泡,盐酸能与碳酸钠反应生成氯化钠、水和二氧化碳;故答案为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
ii.氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故白色沉淀是碳酸钙;生成的氢氧化钠能使酚酞试液变红,故不能确定原固体中是否含有氢氧化钠;故答案为:CaCO3;不能;
iii.若全部是碳酸钠,则加入的氯化钙能与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,生成的;氯化钠的水溶液呈中性,不能使酚酞试液变红,所以,若酚酞不变色,说明溶质全部是碳酸钠;
【反思】久置的氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,则用化学方程式表示2NaOH+CO2═Na2CO3+H2O.
i.根据CO2与NaOH的反应,是气体被吸收进氢氧化钠溶液,二氧化碳气体减少了,则U型管左端的气压减小,从而导致U型管左端液面升高;故填:升高;.
ii.与实验甲相比,同学们认为实验乙更合理,因为:实验一验证了二氧化碳在水中的溶解性;与实验一相比,通过实验二的现象可知,二氧化碳与氢氧化钠溶液发生反应的影响程度远比二氧化碳溶于水所产生的影响大.
故答案为:
【实验和推断】(1)盐酸(合理均可); 2HCl+Na2CO3=2NaCl+H2O+CO2↑;
(2)CaCO3; 不能;
(3)产生白色沉淀; 无色酚酞试液不变色.
【反思】2NaOH+CO2═Na2CO3+H2O;
i.升高;
ii.实验一验证了二氧化碳在水中的溶解性;与实验一相比,通过实验二的现象可知,二氧化碳与氢氧化钠溶液发生反应的影响程度远比二氧化碳溶于水所产生的影响大.
i.氢氧化钠变质生成的是碳酸钠,如果加入A后产生气泡,盐酸能与碳酸钠反应生成氯化钠、水和二氧化碳;故答案为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
ii.氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故白色沉淀是碳酸钙;生成的氢氧化钠能使酚酞试液变红,故不能确定原固体中是否含有氢氧化钠;故答案为:CaCO3;不能;
iii.若全部是碳酸钠,则加入的氯化钙能与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,生成的;氯化钠的水溶液呈中性,不能使酚酞试液变红,所以,若酚酞不变色,说明溶质全部是碳酸钠;
【反思】久置的氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,则用化学方程式表示2NaOH+CO2═Na2CO3+H2O.
i.根据CO2与NaOH的反应,是气体被吸收进氢氧化钠溶液,二氧化碳气体减少了,则U型管左端的气压减小,从而导致U型管左端液面升高;故填:升高;.
ii.与实验甲相比,同学们认为实验乙更合理,因为:实验一验证了二氧化碳在水中的溶解性;与实验一相比,通过实验二的现象可知,二氧化碳与氢氧化钠溶液发生反应的影响程度远比二氧化碳溶于水所产生的影响大.
故答案为:
【实验和推断】(1)盐酸(合理均可); 2HCl+Na2CO3=2NaCl+H2O+CO2↑;
(2)CaCO3; 不能;
(3)产生白色沉淀; 无色酚酞试液不变色.
【反思】2NaOH+CO2═Na2CO3+H2O;
i.升高;
ii.实验一验证了二氧化碳在水中的溶解性;与实验一相比,通过实验二的现象可知,二氧化碳与氢氧化钠溶液发生反应的影响程度远比二氧化碳溶于水所产生的影响大.
点评:本题考查了从反应物和生成物的状态变化入手,注意到反应引起气压的变化,将化学和物理结合起来.所以化学不是一门单独存在的学科,化学和物理是相互联系的,解决化学问题可以应用物理知识.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 24、如图,某兴趣小组同学做了以下实验.请回答有关 问题.
24、如图,某兴趣小组同学做了以下实验.请回答有关 问题.
