题目内容
兴趣小组的同学在开展“废物利用、减少污染”的活动中,取某工厂合金废料(含铝、铁、铜)进行如下实验:
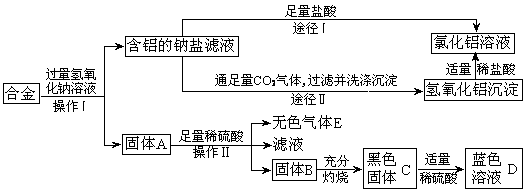
(1)操作Ⅱ的名称是 ;该操作需用到的铁制仪器为 。
(2)固体A的成分是 ;氢氧化铝沉淀与稀盐酸反应的化学方程式为 。
(3)固体C与稀硫酸反应的方程式为 。
(4)图中由含铝的钠盐制备氯化铝有两种途径,你认为合理的途径是 (填:“Ⅰ”或“Ⅱ”),理由是 。

(1)操作Ⅱ的名称是 ;该操作需用到的铁制仪器为 。
(2)固体A的成分是 ;氢氧化铝沉淀与稀盐酸反应的化学方程式为 。
(3)固体C与稀硫酸反应的方程式为 。
(4)图中由含铝的钠盐制备氯化铝有两种途径,你认为合理的途径是 (填:“Ⅰ”或“Ⅱ”),理由是 。
(1)过滤 铁架台
(2)铁、铜(或Fe、Cu) Al(OH)3 + 3HCl = AlCl3 + 3H2O
(3)CuO + H2SO4 = CuSO4 +H2O
(4)Ⅱ 途径Ⅱ没有引入新的杂质,得到的是纯净的氯化铝溶液(或途径Ⅰ引入了杂质钠盐,得到的氯化铝不纯净。合理表述均给分。)
(2)铁、铜(或Fe、Cu) Al(OH)3 + 3HCl = AlCl3 + 3H2O
(3)CuO + H2SO4 = CuSO4 +H2O
(4)Ⅱ 途径Ⅱ没有引入新的杂质,得到的是纯净的氯化铝溶液(或途径Ⅰ引入了杂质钠盐,得到的氯化铝不纯净。合理表述均给分。)
试题分析:通过流程图可以看出,固体A与稀硫酸反应后经过操作Ⅱ后得到了固体和液体,很明显操作Ⅱ是过滤,过滤操作需要烧杯、玻璃棒、漏斗和铁架台四种仪器,在这些仪器中只有铁架台是铁制的;从流程图可以看出,合金(含有铁、铜、铝)经过氢氧化钠溶液和操作I后,得到了含有铝的钠盐溶液和固体A,很明显铝与氢氧化钠溶液反应掉了,且氢氧化钠溶液是过量的,所以铝全部进到了溶液中,固体A中含有铁和铜;固体A与足量的稀硫酸反应其实是固体中的铁与稀硫酸反应,得到的固体B是铜,铜经过灼烧得到的黑色固体是氧化铜;对比得到氯化铝的两条途径可以发现,第一条途径中不但能够得到氯化铝,而且产物中含有氯化钠和氯化氢等杂质,而第二条途径得到的氯化铝较为纯净。

练习册系列答案
相关题目