题目内容
【题目】一个烧杯中盛有一定量盐酸和氯化铜的混合溶液,已知其中盐酸溶质的质量为3.65克,小明为了测定原混合溶液中氯化铜的质量如图1,进行下列实验.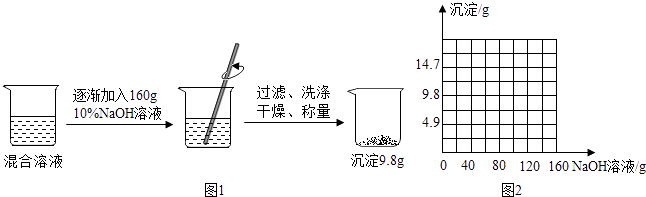
(1)请根据NaOH的化学式计算氧元素和氢元素的质量之比为 , NaOH的相对分子质量为
(2)求原混合溶液中氯化铜的质量(写出计算过程);(CuCl2+2NaOH=Cu(OH)2↓+2NaCl)
(3)请在图2中绘制生成沉淀质量与氢氧化钠溶液质量的关系图.(请用黑色签字笔作图)
【答案】
(1)16:1,40
(2)解:设原混合溶液中氯化铜的质量为x,氯化铜消耗氢氧化钠溶液的质量为y.
CuCl2 + | 2NaOH= | Cu(OH)2↓+2NaCl |
135 | 80 | 98 |
x | y×10% | 9.8g |
![]()
x=13.5g
![]()
y=80g
答:原混合溶液中氯化铜的质量为13.5g
(3)解:盐酸消耗的氢氧化钠溶液的质量为z.
HCl+ | NaOH=2NaCl+H2O |
36.5 | 40 |
3.65g | z×10% |
![]()
z=40g
所以当恰好完全反应时消耗氢氧化钠溶液的质量=40g+80g=120g,生成沉淀的质量为9.8g.
生成沉淀质量与氢氧化钠溶液质量的关系图为:
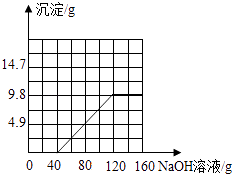
【解析】解:(1)NaOH中氧元素和氢元素的质量之比=16:1;NaOH的相对分子质量=23+16+1=40;故填:16:1;40;
根据化学式计算分析,根据化学式可以求算元素质量比,即相对原子质量![]() 原子个数之比;根据化学方程式计算分析,利用方程式进行计算时,要先写出有关反应方程式,根据方程式量的关系找出相关物质的相对质量比,再从题中找出已知物质的质量,利用相对质量比与实际质量比相等利出比例式求解,注意溶液之间的反应,参加反应的物质为溶液中的溶质,代入方程式中的质量必须是参加反应或生成的纯净物的质量。
原子个数之比;根据化学方程式计算分析,利用方程式进行计算时,要先写出有关反应方程式,根据方程式量的关系找出相关物质的相对质量比,再从题中找出已知物质的质量,利用相对质量比与实际质量比相等利出比例式求解,注意溶液之间的反应,参加反应的物质为溶液中的溶质,代入方程式中的质量必须是参加反应或生成的纯净物的质量。

练习册系列答案
相关题目