题目内容
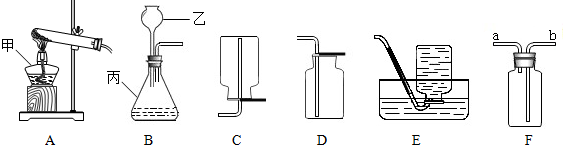
如图是几种常见的实验装置:
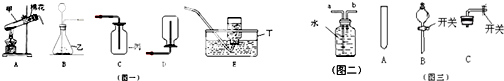
(1)指出仪器名称:甲
(2)如果用高锰酸钾制取氧气,应选用(图一)中的
(3)小明用改进后的装置制取氧气,写出反应的文字表达式
如果他要收集干燥的氧气,可选用(图一)中的
(4)小华想用过氧化氢和二氧化锰制取氧气,她应选用(图一)中
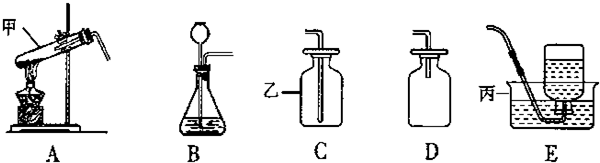
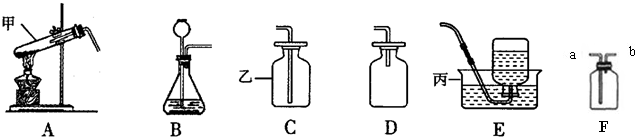
(5)当过氧化氢接触到二氧化锰后,反应便立即开始不能人为控制其速度.如果你稍改变所选择装置,便可控制其反应速度,请从(图三)的仪器中选择一种更换小华选择的装置中一种仪器,以达到控制反应速度的目的,你选择的仪器是
实验结束后,通过相互交流,你认为是

(1)指出仪器名称:甲
试管
试管
乙锥形瓶
锥形瓶
丙集气瓶
集气瓶
丁水槽
水槽
(2)如果用高锰酸钾制取氧气,应选用(图一)中的
A
A
(填序号)作为发生装置,但此装置有不足之处,请指出其中的错误:试管口向上倾斜
试管口向上倾斜
.(3)小明用改进后的装置制取氧气,写出反应的文字表达式
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
高锰酸钾
锰酸钾+二氧化锰+氧气
| 加热 |
如果他要收集干燥的氧气,可选用(图一)中的
C
C
(填序号);如果想要收集一瓶较为纯净的氧气,可选用(图一)中的E
E
(填序号).(4)小华想用过氧化氢和二氧化锰制取氧气,她应选用(图一)中
B
B
作为发生装置,写出该方法制取氧气的文字表达式过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
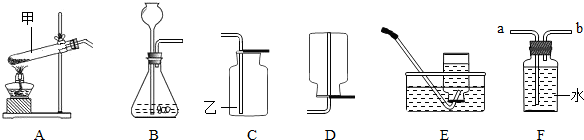
.如果她选用(图二)中的装置收集一瓶氧气,则收集时气体应从导管口的| 二氧化锰 |
b
b
端(填“A”或“b”)通入.(5)当过氧化氢接触到二氧化锰后,反应便立即开始不能人为控制其速度.如果你稍改变所选择装置,便可控制其反应速度,请从(图三)的仪器中选择一种更换小华选择的装置中一种仪器,以达到控制反应速度的目的,你选择的仪器是
B
B
(填序号),它更换原装置中的长颈漏斗
长颈漏斗
(填名称).实验结束后,通过相互交流,你认为是
小华
小华
(填小明或小华)的方法更好,理由是操作方便
操作方便
,不需加热(合理均可)
不需加热(合理均可)
.分析:(1)依据常用仪器回答;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故选A;加热固体药品时试管口应向下倾斜;
(3)依据高锰酸钾分解的反应原理书写表达式;收集干燥的气体通常用排空气法,收集较纯净的气体通常用排水法,据此分析,并结合氧气的性质解答;
(4)用过氧化氢和二氧化锰制取氧气,不需加热,属于固液常温型,故选B;并依据过氧化氢分解的反应原理书写表达式;氧气的密度比水小,并结合装置特点分析解答;
(5)分液漏斗可控制液体的滴加速度,从而达到控制反应速率的目的;根据高锰酸钾和过氧化氢制取氧气的反应及所用装置分析其优缺点.
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故选A;加热固体药品时试管口应向下倾斜;
(3)依据高锰酸钾分解的反应原理书写表达式;收集干燥的气体通常用排空气法,收集较纯净的气体通常用排水法,据此分析,并结合氧气的性质解答;
(4)用过氧化氢和二氧化锰制取氧气,不需加热,属于固液常温型,故选B;并依据过氧化氢分解的反应原理书写表达式;氧气的密度比水小,并结合装置特点分析解答;
(5)分液漏斗可控制液体的滴加速度,从而达到控制反应速率的目的;根据高锰酸钾和过氧化氢制取氧气的反应及所用装置分析其优缺点.
解答:解:(1)依据常用仪器可知甲、乙、丙、丁四种仪器分别是:试管、锥形瓶、集气瓶、水槽;
故答案为:试管;锥形瓶;集气瓶;水槽;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故选A;加热固体药品时试管口应向下倾斜,而图示中试管口高于试管底部,会引起冷凝水倒流引起试管炸裂;
故答案为:A;试管口向上倾斜;
(3)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的表达式是高锰酸钾
锰酸钾+二氧化锰+氧气;收集干燥的气体通常用排空气法,氧气的密度比空气大,故选C;氧气不易溶于水,所以收集较纯净的气体可用排水法;
故答案为:高锰酸钾
锰酸钾+二氧化锰+氧气;C;E;
(4)用过氧化氢和二氧化锰制取氧气,不需加热,属于固液常温型,故选B;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的文字表达式是过氧化氢
水+氧气;氧气的密度比水小,所以应从b端进入,水被挤压到集气瓶底部排出,从而收集到氧气;
故答案为:B;过氧化氢
水+氧气;b;
(5)分液漏斗可控制液体的滴加速度,从而达到控制反应速率的目的,所以要控制反应速度,可用分液漏斗代替长颈漏斗;用过氧化氢制取氧气与利用高锰酸钾制取氧气具有不需加热,节约能源,操作方便等优点,所以小华的方法更好;
故答案为:B;长颈漏斗;小华;操作方便;不需加热(合理均可)
故答案为:试管;锥形瓶;集气瓶;水槽;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故选A;加热固体药品时试管口应向下倾斜,而图示中试管口高于试管底部,会引起冷凝水倒流引起试管炸裂;
故答案为:A;试管口向上倾斜;
(3)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的表达式是高锰酸钾
| 加热 |
故答案为:高锰酸钾
| 加热 |
(4)用过氧化氢和二氧化锰制取氧气,不需加热,属于固液常温型,故选B;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的文字表达式是过氧化氢
| 二氧化锰 |
故答案为:B;过氧化氢
| 二氧化锰 |
(5)分液漏斗可控制液体的滴加速度,从而达到控制反应速率的目的,所以要控制反应速度,可用分液漏斗代替长颈漏斗;用过氧化氢制取氧气与利用高锰酸钾制取氧气具有不需加热,节约能源,操作方便等优点,所以小华的方法更好;
故答案为:B;长颈漏斗;小华;操作方便;不需加热(合理均可)
点评:本题针对实验室制取氧气考查的知识点比较综合,涉及到实验仪器、注意事项、反应原理、装置选取、评价等知识,要在掌握知识的基础上根据题意细心分析解答.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目