题目内容
【题目】下列三个实验均可证明CO2能与NaOH溶液反应.
实验Ⅰ:用试管集满CO2,迅速加入NaOH溶液、塞紧橡皮塞,充分振荡,静置.
(1)实验后打开橡皮塞时,听到响亮的“啵”声,其原因是实验后试管中的气压 (填“变大”或“变小”);
(2)对静置后的溶液进行下列操作,由对应的现象可推知CO2与NaOH溶液一定反应的是 (填序号).
A.滴加酚酞,溶液变为红色
B.滴加少量稀盐酸,不产生气泡
C.滴加少量氯化钡溶液,产生白色沉淀
实验Ⅱ:在8.0g NaOH固体中加入适量95%的乙醇溶液,配制成饱和NaOH的乙醇溶液,向该溶液中通入CO2,直至产生白色沉淀Na2CO3.
(1)某托盘天平标尺的最大刻度为1g,配备有1g、2g、5g和10g四种砝码若干个,用该天平称取8.0g NaOH固体时,所需砝码总数为 个;
(2)实验Ⅱ利用的原理是: 影响物质的溶解性.
实验Ⅲ:如图所示,将5mL溶质质量分数为10%的NaOH溶液(ρ≈1.1g/mL)缓慢、全部注射入瓶中,观察到酒精倒流入瓶中,最终瓶中剩余5mL气体.此实验条件下,1体积水约可溶1体积CO2,CO2不溶于酒精,ρ(CO2)≈2gL.
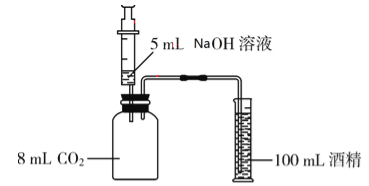
(1)实验时 (填“能”或“不能”)用水代替量筒中的酒精;
(2)实验时将NaOH溶液缓慢注射入瓶中的原因是 ;
(3)根据上述实验可推知:与NaOH溶液反应的CO2约为 (取整数)mL;
(4)理论上,上述5mL NaOH溶液与足量CO2反应都转化为Na2CO3时,参加反应的CO2的体积大约为多少毫升?(写出计算过程,结果取整数)
(5)实际上,上述NaOH溶液吸收的CO2偏少,其原因可能是 (填序号).
A.CO2不纯
B.装置漏气
C.NaOH与CO2化合生成了NaHCO3
d.倒流入瓶中的酒精干扰了NaOH溶液对CO2的吸收.
【答案】
实验Ⅰ.
(1)变小;
(2)c;
实验Ⅱ.(1)3;(2)溶剂的种类;实验Ⅲ.(1)不能;(2)防止二氧化碳气体从导管逸出;(3)75;(4)151;(5)a、b、d
【解析】
试题分析:实验Ⅰ.(1)CO2能与氢氧化钠溶液反应,气体变少,试管内的压强减小;(2)a、要证明CO2与NaOH溶液一定发生反应,只要证明反应后的溶液中含有Na2CO3即可.Na2CO3和NaOH溶液都呈碱性,因此无论CO2与氢氧化钠溶液是否反应,都会是无色酚酞试液变红,故a错误;b、如果NaOH溶液过量,滴加少量的稀盐酸会先与NaOH溶液反应,不会产生气泡,应滴加过量的稀盐酸,观察是否有气泡产生才行,故b错误;c、氯化钡溶液不能与氢氧化钠溶液反应,如果有白色沉淀生成,说明一定含有碳酸钠,也就证明CO2与NaOH溶液一定发生了反应,故c正确;实验Ⅱ.(1)8g=1g+2g+5g,所以需要3个砝码;(2)氢氧化钠水溶液和氢氧化钠乙醇溶液中溶质种类相同,而溶剂种类不同;实验Ⅲ.(1)二氧化碳能溶于水而不能溶液乙醇;(2)为了使二氧化碳能与氢氧化钠溶液充分反应,防止二氧化碳气体从导管溢出,实验时应将氢氧化钠溶液缓缓注入注射器中;(3)进入酒精的体积就是二氧化碳的体积,80mL二氧化碳气体反应后还剩余5mL,说明反应了75mL;(4)NaOH的质量为1.1g/mL×5/mL×10%=0.55g;设参加反应的二氧化碳的质量为x
CO2+2NaOH═Na2CO3+H2O
44 80
x 0.55g
![]()
x=0.3025g
二氧化碳的体积为![]() =0.15125L=151mL.
=0.15125L=151mL.
(5)CO2不纯和装置漏气、酒精倒流到瓶中都会使瓶中二氧化碳变少,从而氢氧化钠溶液吸收的二氧化碳就偏少.故答案为:实验Ⅰ.(1)变小;(2)c;实验Ⅱ.(1)3;(2)溶剂的种类;实验Ⅲ.(1)不能;(2)防止二氧化碳气体从导管逸出;(3)75;(4)151;(5)a、b、d.

 智能训练练测考系列答案
智能训练练测考系列答案