题目内容
【题目】如图所示的四个图象,能正确反映对应变化关系的是( )
A.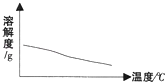
Ca(OH)2的溶解度与温度的变化曲线
B.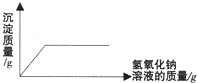
向硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
C.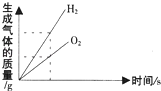
水的电解
D.
分别向等质量的镁和铜固体中逐滴加入盐酸
【答案】A
【解析】解:
A、氢氧化钙的溶解度随温度的升高而减小.故正确;
B、向硫酸和硫酸铜的混合溶液中滴加NaOH溶液,氢氧化钠先和稀硫酸反应,等到稀硫酸反应完毕后,氢氧化钠再和硫酸铜反应生成氢氧化铜沉淀,所以一开始没有沉淀,等到稀硫酸反应完后有沉淀生成,硫酸铜反应完后沉淀不再增加,为一定值,故错误;
C、通电分解水时产生氢气的体积是氧气的二倍,质量比为1:8,故错误;
D、根据金属活动性顺序可知:铜在氢的后面与酸不反应,故错误.
答案:A
【考点精析】解答此题的关键在于理解电解水实验的相关知识,掌握电解水的实验:A.装置―――水电解器B.电源种类---直流电C.加入硫酸或氢氧化钠的目的----增强水的导电性D.化学反应:2H2O=== 2H2↑+ O2↑,以及对固体溶解度的影响因素的理解,了解影响固体溶解度的因素:①溶质、溶剂的性质(种类) ②温度:大多数固体物的溶解度随温度升高而升高;如KNO3;少数固体物质的溶解度受温度的影响很小;如NaCl;极少数物质溶解度随温度升高而降低.如Ca(OH)2.

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
