题目内容
【题目】21世纪是钛的世纪,利用钛白粉(TiO2)生产海绵钛(Ti)的工艺流程如图所示。下列叙述不正确的是( )
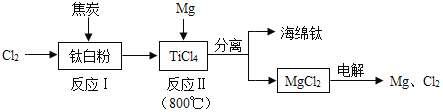
A. 反应I除生成TiCl4以外,还生成一种可燃性气体,该气体应该是CO
B. 反应II的原理是TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
C. 反应II需在氩气环境中进行,目的是防止镁被氧化,不能用氮气来代替氩气
D. 该工艺流程中可以循环使用的物质为氯气
【答案】D
【解析】
A、根据质量守恒定律,化学反应前后元素的种类不变,反应I除生成TiCl4以外,还生成一种可燃性气体,故该气体应该是CO,此选项正确;
B、根据反应的工艺流程,反应II的原理是TiCl4+2Mg![]() Ti+2MgCl2,此选项正确;
Ti+2MgCl2,此选项正确;
C、反应II需在氩气环境中进行,目的是防止镁被氧化,因为镁能与氮气反应,故不能用氮气来代替氩气,此选项正确;
D、该工艺流程中Mg和Cl2既是反应物又是生成物,所以可以循环使用的物质为氯气和镁,此选项错误。故选D。

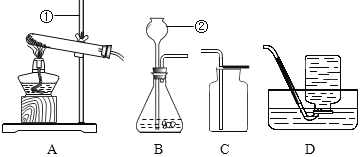
【题目】(1)如图是实验室制取气体的一些装置,据图回答:
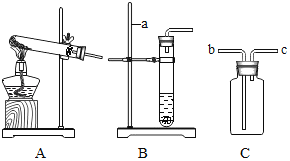
①如图仪器a的名称是_____。
②用高锰酸钾制取氧气的化学方程式是_____。若用C装置收集氧气,验满时,应将带火星的木条放在_____(填“b”或“c”)端导管口,若木条复燃,说明氧气已满。
(2)某校化学兴趣小组在学完碱的化学性质后,做了澄清石灰水和稀盐酸反应的实验,并将废液倒入一洁净的废液缸中,进行了如下探究:
探究Ⅰ:甲同学在做实验时没有观察到明显现象,于是对澄清石灰水和稀盐酸能否发生反应表示怀疑,乙同学认为,甲同学实验时应先向澄淸石灰水中滴几滴酚酞试液,再滴加适量的稀盐酸,当观察到_____时,就可以说明两种物质能发生反应。
探究Ⅱ:废液中溶质的成分是什么?
(做出猜想)
猜想一:CaCl2
猜想二:CaCl2、HCl
猜想三:CaCl2、HCl、Ca(OH)2
你的猜想:_____
丙同学认为猜想三是错误的,理由是_____(用化学方程式解释)。
(实验设计)
设计者 | 实验操作 | 实验现象 | 实验结论 |
丁同学 | 取少量废液于一支试管中,向其中加入足量的碳酸钠溶液 | 有白色沉淀生成 | 猜想一正确 |
戊同学 | 取几粒锌粒于一支试管中,向其中加入少量废液 | _____ | 猜想二正确 |
(评价与反思)请判断以上设计的两个方案中,_____同学的方案合理,请分析另一个方案不合理的理由:_____。
(表达与交流)若实验证明猜想二是正确的,你认为该废液来经处理直接倒入下水道,可能造成的危害是_____(填一点)。
【题目】(1)元素周期表是化学学习和研究的重要工具。下图是元素周期表的一部分。
1H 1.008 | 2He 4.003 | ||||||
3Li 6.941 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10Ne 20.18 |
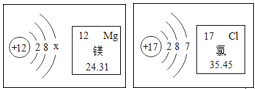
11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
①表中查出硅(Si)元素的相对原子质量为_____;
②9号元素与12号元素形成化合物的化学式为_____;
③11号元素至18号元素同属第三周期,从核外电子排布来看你发现的规律是_____。
(2)在化学反应中,反应物中某元素的化合价在反应后如果增加,则该物质是还原剂,如果是减少的则该物质是氧化剂。请判断反应:2Na+Cl2![]() 2NaCl中,还原剂是_____。
2NaCl中,还原剂是_____。