题目内容
【题目】根据问题回答
(1)用化学符号填空:
①地壳中含量最多的元素是________;
②生物体中含量最多的物质是__________;
③氯化钠中阴离子的符号_____;
④分析过氧化氢(H2O2)和过氧化钠(Na2O2)中氧元素的化合价,写出过氧化钙的化学式为___________。
(2)如图为某化学反应的微观示意图,请回答。

①、在上述反应中不变的粒子是_______(填“分子”或“原子”)。
②、在A、B、C、D中属于单质的是________________(填字母)。
③、一个C分子是由_____________个原子构成的。
④物质A中碳元素的化合价是_____________。
(3)下图是1一18号元素中部分粒子的结构示意图
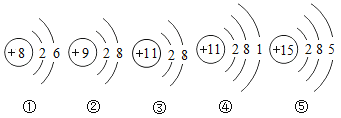
其中属于同种元素的是___________(填序号); 属于阴离子的是 ___________(用粒子符号表示);⑤的原子核内的中子数比核外电子数多1个,则它的相对原子质量是__________。
【答案】O H2O Cl- CaO2 原子 B 9 +2 ③④ F- 31
【解析】
(1)①地壳中含量最多的元素是氧元素,氧元素的符号为O;
②生物体中含量最多的物质是水,化学式为:H2O;
③氯化钠中阴离子是氯离子,符号是Cl-;
④过氧化氢(H2O2)和过氧化钠(Na2O2)中氧元素的化合价的-1价,故过氧化钙的化学式为CaO2。
(2)①化学反应的过程中不变的粒子是原子。
②图B中物质只有一种元素组成,是单质,故选B。
③由图可知,一个C分子是由6个氢原子,2个碳原子,1个氧原子构成,故共有9个原子。
④物质A是一氧化碳,化学式为CO,一氧化碳中碳元素的化合价为+2价。
(3)图中③④的质子数都是11,属于同种元素。②中质子数小于核外电子数,故是阴离子,离子符号为F-。由图⑤可知,该原子的质子数是15,该原子的原子核内的中子数比核外电子数多1个,故中子数是16,则它的相对原子质量为15+16=31。

 初中暑期衔接系列答案
初中暑期衔接系列答案