题目内容
【题目】某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
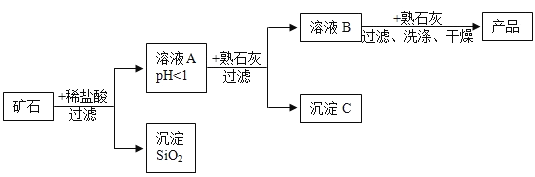
(1)溶液A中共含有________ 种阳离子;
(2)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为_________ ;
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.5 | 4.2 | 8.6 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(3)溶液B中一定含有的溶质为__________(填化学式);
(4)写出溶液B中加入熟石灰,生成产品的化学方程式:______。
【答案】4 6.7-8.6 MgCl2和CaCl2 MgCl2+Ca(OH)2=Mg(OH)2↓+ CaCl2
【解析】
(1)组成矿石的四种氧化物中仅SiO2不与盐酸反应,其余三种均能反应:MgO+2HCl═MgCl2+H2O、Fe2O3+6HCl═2FeCl3+3H2O、CuO+2HCl═CuCl2+H2O,溶液A的pH<1,说明反映后溶液呈强酸性,盐酸过量,因此溶液A中的阳离子有Mg2+、Fe3+、Cu2+、H+;
(2)为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为6.7~8.6,即必须把pH控制在氯化铁、氯化铜能完全沉淀、但氯化镁不能沉淀的范围内;
(3)当B溶液的pH在6.7~8.6时,铜离子、铁离子已经完全沉淀,镁离子没有形成沉淀,所以溶液B中一定含有的溶质为氯化镁和反应生成的氯化钙,化学式分别是MgCl2、CaCl2;
(4)氯化镁和氢氧化钙反应能生成氢氧化镁沉淀和氯化钙,反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案