题目内容
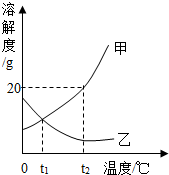 (2013?莆田)如图是甲、乙两种固体物质的溶解度曲线.
(2013?莆田)如图是甲、乙两种固体物质的溶解度曲线.(1)
t1
t1
℃时,甲和乙的溶解度相等.(2)乙的饱和溶液从t2℃降到t1℃时,乙的溶液为
不饱和
不饱和
(填“饱和”或“不饱和”)溶液.(3)t2℃时,甲的饱和溶液中溶质的质量分数为
16.7%
16.7%
(精确到0.1%).(4)t2℃时,将100g10%的甲溶液加水稀释成溶质质量分数为5%的溶液,应加水
100
100
g.分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)据乙的溶解度随温度的变化情况分析解答;
(3)饱和溶液中溶质的质量分数=
×100%及该温度下甲的溶解度分析解答;
(4)据溶液稀释前后溶质的质量相等进行计算.
(2)据乙的溶解度随温度的变化情况分析解答;
(3)饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
(4)据溶液稀释前后溶质的质量相等进行计算.
解答:解:(1)t1℃时甲和乙的溶解度曲线交于一点,二者的溶解度相等;
(2)乙的溶解度随温度的降低而增大,所以乙的饱和溶液从t2℃降到t1℃时,乙的溶液变为不饱和溶液;
(3)t2℃时甲的溶解度是20g,所以甲的饱和溶液中溶质的质量分数为:
×100%≈16.7%;
(4)t2℃时,将100g10%的甲溶液加水稀释成溶质质量分数为5%的溶液,设应加水的质量为x,则有100g×10%=(100g+x)×5%,解得x=100g;
故答案为:(1)t1;(2)不饱和;(3)16.7%;(4)100.
(2)乙的溶解度随温度的降低而增大,所以乙的饱和溶液从t2℃降到t1℃时,乙的溶液变为不饱和溶液;
(3)t2℃时甲的溶解度是20g,所以甲的饱和溶液中溶质的质量分数为:
| 20g |
| 120g |
(4)t2℃时,将100g10%的甲溶液加水稀释成溶质质量分数为5%的溶液,设应加水的质量为x,则有100g×10%=(100g+x)×5%,解得x=100g;
故答案为:(1)t1;(2)不饱和;(3)16.7%;(4)100.
点评:本题考查了对溶解度概念的了解、溶解度曲线的意义和应用,及饱和溶液中溶质质量分数的计算方法,能较好考查学生分析解决问题的能力.

练习册系列答案
相关题目
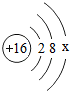 (2013?莆田)如图所示是硫原子的结构示意图.
(2013?莆田)如图所示是硫原子的结构示意图. (2013?莆田质检)如图是甲、乙两种固体物质的溶解度曲线.下列叙述中错误的是( )
(2013?莆田质检)如图是甲、乙两种固体物质的溶解度曲线.下列叙述中错误的是( )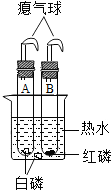 (2013?莆田质检)如图所示的实验装置,用于探究可燃物燃烧的条件.
(2013?莆田质检)如图所示的实验装置,用于探究可燃物燃烧的条件.