题目内容
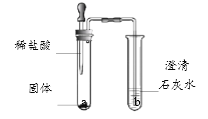
【题目】某化学兴趣小组对一石灰石样品中碳酸钙的质量分数进行实验测定,取12g样品于烧杯中加入足量的稀盐酸放在天平上观察并记录反应过程中天平示数变化如下
反应时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
烧杯及所盛物质总质量/g | 115.0 | 114.0 | 113.0 | 112.0 | 111.2 | 110.9 | 110.7 | 110.6 | 110.6 | 110.6 |
试计算:该石灰石样品中CaCO3的质量分数。(计算结果精确至0.1%)
【答案】83.3%
【解析】解:由题中数据知反应共产生CO2的质量为115.0g-110.6g=4.4g
设石灰石样品中CaCO3的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
![]()
x=10g
该石灰石样品中碳酸钙质量分数![]() ×100%≈83.3%
×100%≈83.3%
答:该石灰石样品中CaCO3的质量分数约为83.3%。

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】请从A或B两题中任选1个作答,若两题均作答,按A计分。
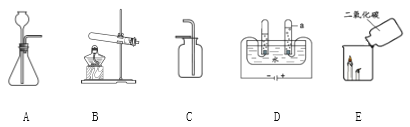
A | B |
(1)实验室用高锰酸钾制取氧气,选取的发生装置是______。 (2)实验室用高锰酸钾制取氧气的化学方程式为___________________。 (3)D中试管a中产生的气为____。 | (1)实验室制取二氧化碳,选取的发生装置是______。 (2)实验室制取二氧化碳的化学方程式为________________。 (3)E中观察到的现象是________。 |
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
【查阅资料】CaC12 滚液显中性
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I:只有CaC12 猜想II:有__________
猜想III:有CaC12和Ca(OH)2 猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________________。
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
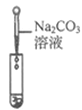
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_______。
【题目】已知硝酸钾在不同温度下的溶解度如下表:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
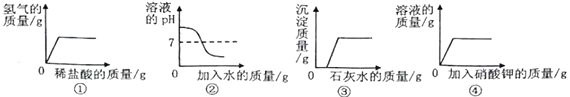
甲是80℃含有100 g水的KNO3溶液,操作过程如下图所示。以下分析错误的是
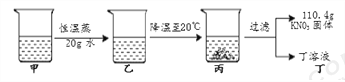
A. 甲、乙、丙、丁四种溶液中,饱和溶液只有2种
B. 甲到乙的过程中,溶质质量没有改变
C. 甲溶液中,溶剂与溶质的质量比为25: 34
D. 甲溶液冷却时,开始析出固体的温度在60℃~70℃之间