题目内容
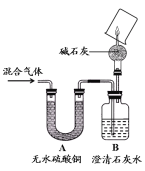
【题目】取25g粉碎的石灰石样品(杂质不溶于水也不与盐酸反应),放入小烧杯中,慢慢加入一定浓度的稀盐酸,测得稀盐酸的用量与剩余固体的质量关系如图。
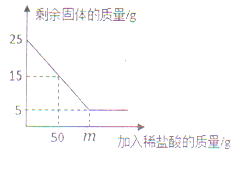
请回答下列问题:
(1)图中m=___________ ;石灰石样品中CaCO3的质量分数= ___________________ ;
(2)求样品完全反应生成二氧化碳的质量____________(写出计算过程)。
【答案】 100 80% 8.8g
【解析】(1)由图可知固体的质量减少25g-15g=10g时,消耗盐酸的质量为50g;当固体的质量减少25g-5g=20g时,消耗盐酸的质量为100g;所以m=100;
石灰石样品中CaCO3的质量=25g-5g=20g;石灰石样品中CaCO3的质量分数为![]() ×100%=80%;
×100%=80%;
(2)解:设生成CO2的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
20g x
![]()
x=8.8g
答:生成CO2的质量为8.8g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表:
物质 | W | G | H | P |
反应前质量/g | 18 | 1 | 2 | 32 |
反应后质量/g | 待测 | 26 | 2 | 12 |
对该反应的认识正确的是![]()
![]()
A. W待测值是13
B. 该反应是分解反应
C. P是生成物
D. 物质H是该反应的催化剂