题目内容
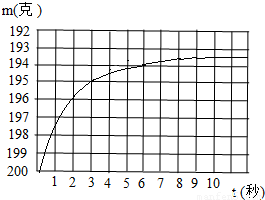
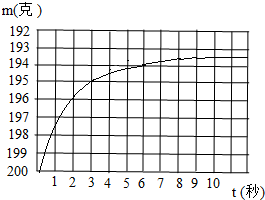 向敞口烧瓶中加入12、6克碳酸氢钠,再加入浓度为14、7%的硫酸溶液100克,烧瓶连同药品的起始质量为200克,用自动计时和称装置每秒钟测量一次烧怀连同药品的质量,所得质量与时间的关系如曲线所示.试通过计算并对照曲线回答:碳酸氢钠反应到一半时所用的时间约是多少秒?往反应停止后的溶液中滴入石蕊试液,试液呈什么颜色?
向敞口烧瓶中加入12、6克碳酸氢钠,再加入浓度为14、7%的硫酸溶液100克,烧瓶连同药品的起始质量为200克,用自动计时和称装置每秒钟测量一次烧怀连同药品的质量,所得质量与时间的关系如曲线所示.试通过计算并对照曲线回答:碳酸氢钠反应到一半时所用的时间约是多少秒?往反应停止后的溶液中滴入石蕊试液,试液呈什么颜色?
分析:写出化学方程式并计算出一半碳酸氢钠参加反应时烧杯连同药品的质量,然后对照图象即可.根据硫酸和碳酸氢钠的质量判断出哪种物质剩余,然后判断滴加石蕊后溶液的颜色.
解答:解:碳酸氢钠的质量是12.6克,所以一半碳酸氢钠的质量=12.6克÷2=6.3克,设生成二氧化碳的质量是X.
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
168 88
6.3克 X
═
得:X=3.3克.
∴一半碳酸氢钠参加反应后烧杯连同药品的质量=200克-3.3克=196.7克.
∴查曲线图可知约为1.2秒.
硫酸的质量=100×14.7%═14.7克,碳酸氢钠的质量是12.6克,设12.6克碳酸氢钠全部参加反应所需硫酸的质量是Y.
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
168 98
12.6克 Y
═
得:Y=7.35克
∵7.35克<14.7克,∴硫酸溶液是过量,因此最后溶液是酸性溶液,则往反应停止后的溶液中滴入石蕊试液,溶液的颜色是红色.
答:碳酸氢钠反应到一半时所用的时间约是1.2秒;往反应停止后的溶液中滴入石蕊试液,溶液的颜色是红色.
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
168 88
6.3克 X
| 168 |
| 88 |
| 6.3克 |
| X |
得:X=3.3克.
∴一半碳酸氢钠参加反应后烧杯连同药品的质量=200克-3.3克=196.7克.
∴查曲线图可知约为1.2秒.
硫酸的质量=100×14.7%═14.7克,碳酸氢钠的质量是12.6克,设12.6克碳酸氢钠全部参加反应所需硫酸的质量是Y.
2NaHCO3+H2SO4═Na2SO4+2H2O+2CO2↑
168 98
12.6克 Y
| 168 |
| 98 |
| 12.6克 |
| Y |
得:Y=7.35克
∵7.35克<14.7克,∴硫酸溶液是过量,因此最后溶液是酸性溶液,则往反应停止后的溶液中滴入石蕊试液,溶液的颜色是红色.
答:碳酸氢钠反应到一半时所用的时间约是1.2秒;往反应停止后的溶液中滴入石蕊试液,溶液的颜色是红色.
点评:掌握化学方程式的计算格式和规范性,学会判断物质过量的方法.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
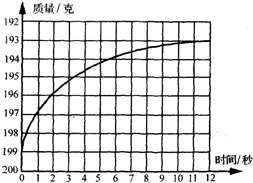 向敞口烧瓶中加入12.6g碳酸氢钠,再加入浓度为14.7%的硫酸溶液100g.烧瓶连同药品的起始质量为200g.用自动计时和称重装置每秒钟测量一次烧瓶连同药品的质量,所得质量与时间的关系如曲线所示.试通过计算并对照曲线回答:
向敞口烧瓶中加入12.6g碳酸氢钠,再加入浓度为14.7%的硫酸溶液100g.烧瓶连同药品的起始质量为200g.用自动计时和称重装置每秒钟测量一次烧瓶连同药品的质量,所得质量与时间的关系如曲线所示.试通过计算并对照曲线回答: