题目内容
【题目】化学与生活密切相关 :
(1)端午节吃粽子是我国的传统习俗,闽南特色粽子的主要原料为大米、肉、咸蛋黄、海蛎干、食盐,主要原料中富含糖类物质的是____________;从营养素的角度看原料中缺少了___________(填蛋白质、维生素、油脂中的一种);
(2)端午还有喝雄黄酒的习俗,雄黄主要含二硫化二砷(As2S2),该物质具有解毒杀虫,燥湿祛痰,截疟之功效,受热易氧化成两种氧化物,其中三氧化二砷(俗称砒霜)毒性很强。写出该氧化反应的化学方程式_____________________。
【答案】 大米 维生素 2As2S2+7O2![]() 2As2O3+ 4SO2或2As2S2+9O2
2As2O3+ 4SO2或2As2S2+9O2![]() 2 As2O3+4 SO3。
2 As2O3+4 SO3。
【解析】本题考查了营养素的来源和化学方程式的书写。
(1)大米中富含淀粉,淀粉属于糖类,肉中富含蛋白质和油脂,咸蛋黄、海蛎干中富含蛋白质,食盐中主要含有氯化钠,氯化钠属于无机盐,闽南特色粽子主要原料中富含糖类物质的是大米;从营养素的角度看原料中缺少了维生素;
(2)二硫化二砷(As2S2) 受热易氧化成两种氧化物。根据质量守恒定律可知,生成的氧化物分别是As2O3和SO2或As2O3和SO3,化学方程式分别为:2As2S2+7O2![]() 2As2O3+ 4SO2,2As2S2+9O2
2As2O3+ 4SO2,2As2S2+9O2![]() 2 As2O3+4 SO3。
2 As2O3+4 SO3。

【题目】“双吸剂”是常用的食品防腐剂,品名为“504双吸剂”,其标签如下图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。

(提出问题)久置固体的成分是什么?
(查阅资料)铁与氯化铁溶液在常温下发生反应。Fe+2FeCl3=3FeCl2
(作出猜想)久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
(实验探究1)甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
⑴取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液。 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 | 固体中一定含有_____和氢氧化钙。 |
⑵另取少量固体放于试管中,滴加足量稀盐酸。 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 | 固体中一定含有____, 一定不含Fe2O3。 |
⑶将步骤⑵中产生的气体通入到澄清的石灰水中。 | _________________ | 固体中一定含有CaCO3。 |
(实验质疑)
⑴乙同学认为甲同学的实验中并不能得出一定含Ca(OH)2的结论,理由是___________;
⑵丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是______________。
(实验探究2)乙、丙同学设计如下实验方案继续验证:
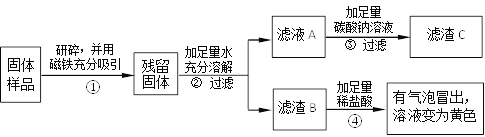
(1)③中反应的化学方程式是______________________;
(2)乙、丙同学实验中又能得出固体样品中一定还含有_________,仍有一种物质不能确定,该物质是_____;
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
(实验结论)综合上述实验及所给数据,久置固体的成分是 ______________________。