题目内容
【题目】下列实验指定容器中的水,其解释没有反映出水的主要作用的是( )
实 验 装 置 |
硫在氧气中燃烧 |
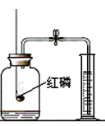
测定空气中氧气含量 |
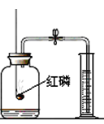
测定空气中氧气含量 |
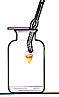
铁丝在氧气中燃烧 |
解释 | 集气瓶中的水:防止集气瓶炸裂 | 集气瓶中的水:更快的吸收白烟 | 量筒中的水:通过水体积的变化得出氧气体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 |
A | B | C | D |
A.AB.BC.CD.D
【答案】A
【解析】
A. 硫在氧气中燃烧,集气瓶中的水是吸收生成的二氧化硫,防止污染空气,此选项错误;
B. 测定空气中氧气含量,集气瓶中的水主要作用是吸收生成物五氧化二磷,此选项正确;
C. 测定空气中氧气含量,量筒中的水主要作用是通过水体积的变化间接测定出氧气体积,此选项正确;
D. 铁丝在氧气中燃烧放出大量的热,会使固体熔化为液体落到集气瓶底部而炸裂瓶底,故集气瓶中的水主要作用是冷却溅落融熔物,防止集气瓶炸裂,此选项正确。
故选A。

【题目】化学教材中“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。请你一起参与他们的探究过程,并填写下列空白。
(问题)氧化铜![]()
![]() 能不能作过氧化氢
能不能作过氧化氢![]() 分解反应的催化剂呢?
分解反应的催化剂呢?
(猜想)______。
(实验验证)
实验 | 实验步骤 | 实验现象 | 实验结论 |
实验一 | 常温下,在试管中加入 | 有少量气泡产生,木条没有复燃 | 常温下 |
实验二 | 常温下,在装有 | 有较多气泡产生,木条复燃 | ______ |
(过论与反思)经过讨论,有的同学认为只有上述两个实验,不能证明CuO能作过氧化氢分解反应的催化剂,还要补充一个探充实验。
实验三:(实验目的)探究______。
(实验步骤)①准确称量![]() 少量
少量![]() 的质量;
的质量;
②重复实验二的步骤;待反应结束,将试管里的物质过滤,洗涤,干燥,称量;
③对比反应前后CuO的质量。
(讨论)如果______,则说明CuO能作过氧化氢分解反应的催化剂。但小茗同学认为,要证明猜想,上述三个实验还不足以说明,还需要再增加一个实验,以验证______。
(实验结论)CuO能作过氧化氢分解反应的催化剂,请写出CuO催化过氧化氢分解的文字表达式:______。
(拓展探究)同种催化剂,你还知道那些因素会影响过氧化氢分解反应的催化效果?假设:______。方案:______。
【题目】在测定空气中氧气含量的实验中,小茗同学采用了如图所示装置:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时交替缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。

(1)在实验加热过程中交替缓慢推动两个注射器活塞的目的是_____。
(2)写出该实验中反应的文字表达式_____。
(3)小茗同学测得结果如下表所示:
反应前注射器气体总体积 | 反应后注射器内气体总体积 |
25mL | 22mL |
由此数据可以推算出他测定的空气中氧气的体积分数_____(填“>"、“=”或“<”)21%。造成该实验出现误差的原因可能是_____(填序号)。
①没有交替缓慢推动两个注射器活塞
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
(4)通过上面的实验你学到的测量混合物中某成分含量的方法是_____。
(5)实验中的一些原因或者装置本身可能导致实验失败,请列举一条:_____。
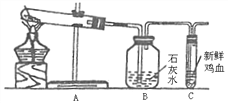
【题目】李老师在实验室制取了两瓶无色气体,分别置于实验台,如下图,请回答下列问题:
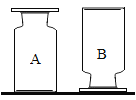
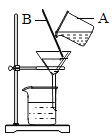
(1)据你所学习的化学知识,结合两种气体的放置情况判断,B气体密度特点是____;A气体可能是_________.
(2)根据你对A气体的判断,完成下列对该气体化学性质探究的实验报告。
实验步骤 | _________ |
实验现象 | _________ |
实验结论 | 该气体是_______________。 |