题目内容
【题目】氯化钠的部分溶解度如下:
温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
溶解度(g/100g水) | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 | 38.0 | 39.2 |
(1)20℃时,15g水中溶解_____g氯化钠刚好形成饱和溶液。
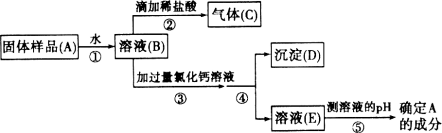
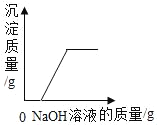
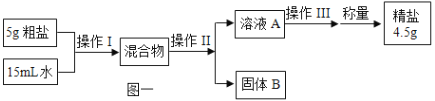
(2)粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是溶液_____(选填“饱和”或“不饱和”);操作Ⅱ是_____。
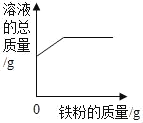
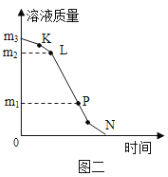
(3)操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是_____(填序号)。
a.m3<20g b.(m2-m1)是减少的水的质量
c.L、P表示的溶液,溶质质量分数相同 d.N点时,停止加热
【答案】5.4 不饱和 过滤 ac
【解析】
(1)20℃时,氯化钠的溶解度是36g,所以15g水中溶解![]() =5.4g氯化钠刚好形成饱和溶液;
=5.4g氯化钠刚好形成饱和溶液;
(2)粗盐提纯最后得到的精盐质量为4.5g,20℃时,15g水中溶解5.4g氯化钠刚好形成饱和溶液,所以溶液A是不饱和溶液,固液分离的操作II是过滤;
(3)a、粗盐中含有不溶性杂质,所以m3<20g,故正确;
b、(m2-m1)是减少的水的质量和析出晶体的质量,故错误;
c、L、P表示的溶液都是不会溶液,所以溶质质量分数相同,故正确;
d、出现较多固体时,停止加热,故错误。
故选:ac。
答案为:(1)5.4;(2)不饱和;过滤;(3)ac。

【题目】空气中氧气含量测定的再认识。
【实验回顾】
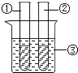
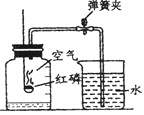
图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
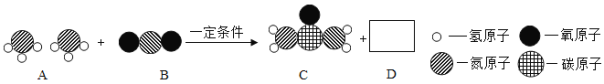
(1)写出红磷燃烧的符号表达式 。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气体的 减小,烧杯中水倒吸到集气瓶。
【问题提出】
有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值往往相差较大。
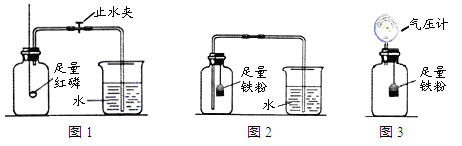
【实验改进】
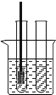
Ⅰ. 甲同学根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量(装置中装铁粉的纸袋浸有浓食盐水,会加速铁生锈)。
Ⅱ. 乙同学经过思考,在图2的基础上设计了图3实验装置,实验测得实验数据如下表:
时间/h | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
压强/KP | 101.6 | 89.7 | 85.4 | 83.3 | 82.2 | 81.] | 81.2 | 81.2 | 81.2 |
【交流表达】
(1)根据表中数据计算,改进后测得空气中氧气的体积分数是 (结果精确到0.1%)。
(2)从实验原理角度分析,图2的实验结果比图1准确度更髙的主要原因是: 。
【实验反思】
许多同学用改进前图1装置得出的结论却也与理论值相差不大,其主要原因是:
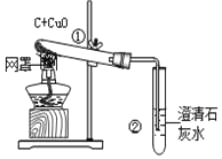
【题目】某同学设计下表所示实验,探究金属铜对H2O2分解速率的影响.
操 作 | 装 置 | 现 象 |
(1).取一个铜丝网,卷成筒形,固定在铁丝上. |
| |
(2).分别向①和②中注入15mL、30%的H2O2溶液,并放入盛有热水的③中. |
| 约1min后可观察到①和②中都有少量气泡产生. |
(3).把铜丝网插入①中. |
| ①中有大量气泡产生,5min后不再有气泡产生;此时②中仍然不断有少量气泡产生. |
回答下列问题:
(1)仪器①的名称是_____;仪器③的名称是_____.
(2)仪器②中实验的目的是_____.
(3)能否可以得出铜可以加快H2O2分解的速率_____(填“是”或“否”),理由是_____
(4)如果用上述实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是_____.
A 称量实验前铜丝网的质量和实验后干燥铜丝网的质量
B 向仪器②中加入二氧化锰
C 将实验后的铜丝网插入AgNO3溶液中
D 将铁丝换成铜丝
E 将过氧化氢溶液加水稀释.