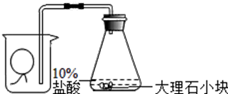
题目内容
【题目】下列实验操作中,不正确的是( )
A. 蒸发食盐水
蒸发食盐水
B.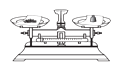 称量固体
称量固体
C.![]() 滴加液体
滴加液体
D.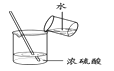 稀释浓硫酸
稀释浓硫酸
【答案】D
【解析】A、蒸发食盐要用玻璃棒不断搅拌,外焰加热,A不符合题意;
B、使用天平称量固体粉末状物质时,在两个托盘上各放一张相同质量的纸,然后把药品放在纸上称量,且左物右码,B不符合题意;
C、使用胶头滴管时要垂直悬空,不伸入试管内,C不符合题意;
D、稀释浓硫酸时不能将水倒入浓硫酸中,防止水浮在上面沸腾溅出,D符合题意.
故答案为:D.
A、为了防止液体飞溅,蒸发操作有大量固体出现时要用玻璃棒搅拌;
B、使用托盘天平要遵循“左物右码”的原则,如果称量粉末状固体,要将固体和砝码分别放在一张完全相同的纸片上;
C、用胶头滴管向试管中滴加液体时,胶头滴管要垂直悬空;
D、稀释浓硫酸时要将浓硫酸倒入水中.

【题目】“绿水青山就是金山银山”,已成为国家意志和全民共识,建设天蓝、地绿、水清的美丽中国,我们任重而道远。使用下列交通工具出行,污染环境最大的是( )
A.氢能源车B.共享单车C.电动汽车D.柴油汽车
【题目】根据所给的仪器回答问题:

(1)I.写出仪器名称,a_、b;
(2)II.某同学用A装置制取氧气时发现试管位置太高,不能用外焰加热,该同学应调节图2中的旋钮 (填“①”或“②”或“③”).
利用改正后的A装置制取氧气,反应的化学方程式: , 若用装置F收集并粗略测出收集O2体积,还需在 (填m或n)端接一个量筒以便测出排出的水的体积。G图是硫在氧气中燃烧的实验,观察到的现象是 , 该反应的化学方程式是;
(3)晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据记录如表所示:
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
2%的H2O2的体积/毫升 | 20 | X |
温度/℃ | 20 | 80 |
①实验2中X的值应为毫升;
②实验中,可通过来比较H2O2分解速率的大小;
③实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因是 .
a、锥形瓶内气体受热膨胀 b、收集到的氧气中混有空气
c、温度较高时水蒸发成水蒸气 d、生成更多的氧气
(4)晓晓从家中拿来一瓶久置的医用过氧化氢溶液来测定该溶液中溶质质量分数.她取出该溶液51 g,加入适量二氧化锰,生成O2的质量与反应时间的关系如图2所示.
Ⅰ、完全反应后生成氧气的质量为 moL.
Ⅱ、计算参与反应的过氧化氢的物质的量 . (写出计算过程)
Ⅲ、这瓶过氧化氢溶液的质量分数为 .