题目内容
【题目】如图是甲,乙,丙三种物质(均不含结晶水)的溶解曲线图.现有t2℃时甲,乙,丙三种物质的饱和溶液(无固体存在).下列说法正确的是( )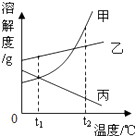
A.t1℃时等质量的三种物质的饱和溶液中溶剂的质量由多到少依次为:乙>丙=甲
B.将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙=甲
C.将温度由t2℃降到t1℃时,析出甲的质量比乙多
D.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯
【答案】D
【解析】A、由溶解度曲线可知,t1℃时甲、乙、丙三种物质的溶解度大小关系是乙>甲=丙,即等质量的溶剂中溶解的乙的量最多,那么等质量的三种物质的饱和溶液中溶剂的质量由多到少依次为:丙=甲>乙,A不符合题意;
B、将温度由t2℃降到t1℃,由于甲和乙的溶解度随温度的降低而减小,故降温后它们的溶解度减小,是t1℃的饱和溶液,溶质质量分数为t1℃的溶质质量分数,即乙>甲;丙的溶解随温度的降低而增大,故降温后丙由饱和溶液变成不饱和溶液,溶质的质量分数不变,故所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙,B不符合题意;
C、甲的溶解度随温度的变化变化较大,故将温度由t2℃降到t1℃时,等质量的甲乙的饱和溶液,析出甲的质量比乙多,C不符合题意;
D、甲的溶解度随温度的变化变化较大,故用降温结晶的方法提纯甲,D符合题意。
所以答案是:D。
【考点精析】解答此题的关键在于理解固体溶解度曲线及其作用的相关知识,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案【题目】小鸣同学特别喜欢化学,经常看一些与化学有关的课外书,有一次阅读化学氧自救器的说明书中,看到人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气后,对自救器内发生的化学反应原理产生了探究欲望。在老师指导下,小鸣与化学兴趣小组的同学们展开了以下两个实验探究活动,请你也参与。
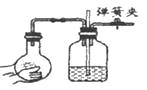
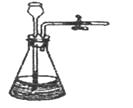
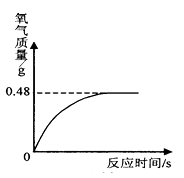
活动Ⅰ:用下图所示的由a、b、c、d组合成的装置和有关药品制取并收集氧气。
活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气还生成什么其他物质?
[老师提示]二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
(1)[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?小强作出了以下两种猜想:
①是一种碱;②是一种碳酸盐。
通过对反应物有关的元素组成的分析,小影同学认为猜想(填序号)一定是错误的,理由是。
(2)[进行实验]同学们通过以下实验验证小强同学的另一个猜想。
实验步骤 | 实验现象 | 实验结论 |
将二氧化碳与超氧化钾反应后的固体 | 猜想是正确的,二氧化碳与超氧化钾反应生成的化合物是(填名称)。 |
(3)[交流与讨论]
小影认为:二氧化碳与超氧化钾反应的化学方程式。