题目内容
在一定条件下,同一反应进行的快慢与反应物的浓度成正比,现用100克溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应速度降低一些而又不影响生成氢气的总量,可向所用硫酸中加入适量的( )
| A、盐酸 | B、氢氧化钠溶液 |
| C、硫酸钾溶液 | D、碳酸钠溶液 |
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:A、盐酸能和镁反应生成氯化镁和氢气;
B、氢氧化钠能和稀硫酸反应生成硫酸钠和水;
C、硫酸钾不能和稀硫酸、镁等物质反应;
D、碳酸钠能和稀硫酸反应生成硫酸钠、水和二氧化碳.
B、氢氧化钠能和稀硫酸反应生成硫酸钠和水;
C、硫酸钾不能和稀硫酸、镁等物质反应;
D、碳酸钠能和稀硫酸反应生成硫酸钠、水和二氧化碳.
解答:解:A、加入盐酸时,盐酸能和镁反应生成氢气,影响生成氢气的质量,因此不能加入盐酸;
B、加入氢氧化钠时,氢氧化钠能和稀硫酸反应消耗稀硫酸,影响生成氢气的质量,因此不能加入氢氧化钠;
C、因为硫酸钾不能和稀硫酸、镁等物质反应,加入硫酸钾时,既能够降低稀硫酸的浓度,减慢反应速率,又不影响氢气的质量;
D、加入碳酸钠时,碳酸钠能和稀硫酸反应消耗稀硫酸,影响生成氢气的质量,因此不能加入碳酸钠溶液.
故选:C.
B、加入氢氧化钠时,氢氧化钠能和稀硫酸反应消耗稀硫酸,影响生成氢气的质量,因此不能加入氢氧化钠;
C、因为硫酸钾不能和稀硫酸、镁等物质反应,加入硫酸钾时,既能够降低稀硫酸的浓度,减慢反应速率,又不影响氢气的质量;
D、加入碳酸钠时,碳酸钠能和稀硫酸反应消耗稀硫酸,影响生成氢气的质量,因此不能加入碳酸钠溶液.
故选:C.
点评:酸具有一些相似的化学性质,例如能使石蕊试液变红色,能和某些金属单质、某些金属氧化物、某些盐、碱反应生成相应的物质.

练习册系列答案
相关题目
生活中的一些问题常会涉及我们课堂上所学习的科学知识,下列叙述中错误的是( )
| A、给发烧病人擦酒精可以降温 |
| B、软质铅笔芯的粉末灌入生锈的锁孔里锁比较容易打开 |
| C、核电站通过核反应发电 |
| D、青少年补钙可以预防甲状腺肿大 |
将下列各组中的物质混合,若每组中最后一种物质过量,充分反应后过滤,则滤纸上仅留下一种不溶性物质(纯净物)的是( )
①氢氧化钠溶液、氯化镁溶液、硝酸;②氯化钡溶液、硝酸钠溶液、稀硫酸;③氯化铜溶液、氯化亚铁溶液、锌粒;④氯化钠溶液、硝酸银溶液、盐酸;⑤硫酸铁溶液、硝酸钠溶液、氢氧化钡溶液.
①氢氧化钠溶液、氯化镁溶液、硝酸;②氯化钡溶液、硝酸钠溶液、稀硫酸;③氯化铜溶液、氯化亚铁溶液、锌粒;④氯化钠溶液、硝酸银溶液、盐酸;⑤硫酸铁溶液、硝酸钠溶液、氢氧化钡溶液.
| A、②④ | B、②③ | C、③⑤ | D、①④ |
空气中含量最多的元素和地壳中含量第二的金属元素及人体中含量最多的元素,共同组成化合物,其化学式可能为( )
| A、Al(NO3)3 |
| B、Fe(NO3)3 |
| C、Fe2O3 |
| D、Fe(NO3)2 |
已知一种锶原子的质子数为38,中子数为37,则这种锶原子的核外电子数为( )
| A、38 | B、37 | C、75 | D、103 |
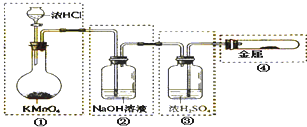 已知KMnO4与浓HCl在常温下反应能产生Cl2,黄绿色易溶于水的氯气有毒性,并能与氢氧化钠溶液反应.若用图示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中存在明显错误的是(不考虑①单元装置)( )
已知KMnO4与浓HCl在常温下反应能产生Cl2,黄绿色易溶于水的氯气有毒性,并能与氢氧化钠溶液反应.若用图示的实验装置来制备纯净、干燥的氯气,并试验它与金属的反应.每个虚线框表示一个单元装置,其中存在明显错误的是(不考虑①单元装置)( )| A、只有④处 |
| B、只有②处 |
| C、只有②和③处 |
| D、②、③、④处 |
下列关于氧气的说法,不科学的是( )
| A、常用带火星的木条来检验空气中的O2 |
| B、空气中的氧气主要来自于植物的光合作用 |
| C、用含有氧元素的物质反应才有可能产生氧气 |
| D、自然界的水中含有一定量的氧气 |
现有未贴上标签的三瓶无色液体,分别是稀硝酸、氯化钠溶液、氢氧化钠溶液,能用①石蕊试液②氢氧化钡溶液③氯化铁溶液④酚酞可以把它们一一区别开的试剂有( )
| A、只有① | B、①② |
| C、①③④ | D、①②③④ |