题目内容
【题目】实验室用10克8%的氢氧化钠溶液和稀硫酸进行中和反应实验,实验过程中溶液的pH变化如图所示:
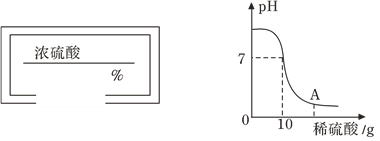
(1)A点溶液的溶质___________。(填化学式)
(2)计算所用的该稀硫酸的质量分数_______?
(3)如果配制100克该稀硫酸所用图中浓硫酸的质量为10克,则图中盛浓硫酸试剂瓶上的标签(已破损)的溶质质量分数应填上___________%。
(4)图中的浓硫酸多次使用后,发现浓度变小了,原因是___________________。
【答案】 Na2SO4,H2SO4 9.8% 98% 浓硫酸吸收了空气中水份
【解析】(1) 氢氧化钠溶液和稀硫酸反应生成硫酸钠和水,A点呈酸性,说明硫酸过量,故溶质为Na2SO4和H2SO4; (2)设参加反应的H2SO4质量![]()
2NaOH + H2SO4 =Na2SO4 +2H2O
80 98
10g×8% ![]()
![]() ×8%=
×8%=![]()
H2SO4%=![]() ×100%=9.8% 答:所用的该稀硫酸的质量分数为9.8%。
×100%=9.8% 答:所用的该稀硫酸的质量分数为9.8%。
(3) 配制100克该稀硫酸所用浓硫酸的质量为10克,设所用浓硫酸的质量分数为y
100g×9.8%=98% y y= 98% (4) 浓硫酸有吸水性,吸收了空气中水而被稀释,导致溶质的质量分数变小。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目