题目内容
【题目】如图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D分别是四种粒子的结构示意图。根据题中信息回答:
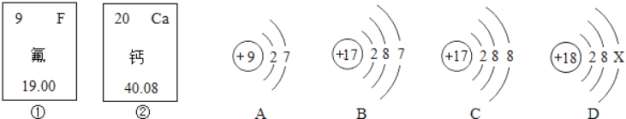
(1)钙原子的核电荷数为_____,氟元素的相对原子质量为_____;
(2)D图中的X=_____;A、B、C、D中属于同种元素的粒子是_____(填序号);
(3)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似_____(填序号);
(4)已知10.0g 第②号元素的单质在足量氧气中燃烧,生成18.0g 纯净的固体产物,则该固体产物的化学式为_____。
【答案】20; 19.00 8; BC B CaO2
【解析】
(1)由元素周期表的信息可知,钙元素的原子序数为20,则钙原子的核电荷数为20;氟元素的相对原子质量为19.00;
(2)E是氩元素,属于稀有气体元素,化学性质很不活泼,不容易得失电子,因此是氩原子,故X=18﹣2﹣8=8;A、B、C、D中属于同种元素的粒子是BC,这是因为BC核内质子数相等;
(3)A粒子的化学性质与A、C、D中B粒子的化学性质相似,这是因为AB的最外层电子数相等,都是7;
(4)②号元素是钙元素,10.0g金属钙在氧气中燃烧生成18.0g纯净的固体产物,则参加反应的氧气的质量为:18.0g-10.0g=8.0g,由质量守恒定律可知,该固体物质中,钙元素与氧元素的质量为10.0g:8.0g,设该化合物的化学式为CaxOy,则:40x:16y=10.0g:8.0g,x:y=1:2,所以该物质的化学式为CaO2。

【题目】某同学为了测定实验室中氯酸钾样品的纯度,取10g该样品与1g二氧化锰混合。加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 10.04 | 9.08 | 8.12 | 8.12 |
(1)完全反应后产生氧气的质量为_____________。
(2)求该样品中氯酸钾的纯度________。