题目内容
【题目】水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要爱护和节约. 
(1)自来水厂在净化水时,常加入活性炭以清除水中异色、异味、其净化原理是利用活性炭的作用.
(2)小娟同学取一杯澄清的自来水,置于洁净的小烧杯中,用酒精灯加热,慢慢蒸发,水分蒸干后,观察到烧杯底部有少许白色固体残留,其原因是;
(3)我国有许多盐碱湖,湖中溶有大量氯化钠和纯碱,已知氯化钠和纯碱的溶解度曲线如图2所示: 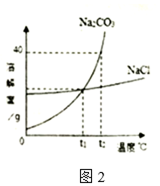
①t2℃时碳酸钠的溶解度氯化钠的溶解度(填“大于”“小于”“等于”之一);
②将t2℃时氯化钠和碳酸钠的饱和溶液均降温到t1℃时,析出氯化钠晶体的质量析出碳酸钠晶体的质量(“大于”“小于”“等于”“无法确定”之一).
③t2℃时将40g碳酸钠固体加入50g水中,所得碳酸钠溶液中溶质与溶剂的质量比为 .
【答案】
(1)吸附
(2)自来水中含有可溶性物质
(3)大于;无法确定;2:5
【解析】解:(1)活性炭有吸附作用,可以吸附一些染料、色素、异味等;所以答案是:吸附;(2)取一杯澄清的自来水,置于洁净的小烧杯中,用酒精灯加热,慢慢蒸发,水分蒸干后,观察到烧杯底部有少许白色固体残留,其原因是:自来水中含有可溶性物质;所以答案是:自来水中含有可溶性物质;(3)由溶解度曲线可知:t2℃时碳酸钠的溶解度大于氯化钠的溶解度;将t2℃时氯化钠和碳酸钠的饱和溶液均降温到t1℃时,析出氯化钠晶体的质量与析出碳酸钠晶体的质量,无法确定大小,因为没有说明饱和溶液的质量;t2℃时将40g碳酸钠固体加入50g水中,所得碳酸钠溶液中溶质与溶剂的质量比=20g:50g=2:5,所以答案是:①大于;②无法确定;③2:5;
【考点精析】解答此题的关键在于理解固体溶解度曲线及其作用的相关知识,掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案