题目内容
【题目】下列排序正确的是( )
A. 空气中物质含量由多到少:O2、N2、CO2
B. 溶液pH值由高到低:HNO3、NaCl、NH3·H2O
C. 金属活动性顺序由强到弱:Zn、Ag、Cu
D. 硫元素质量分数由高到低:Na2S、Na2SO3、Na2SO4
【答案】D
【解析】
A、空气中物质含量由多到少:N2、O2、CO2,故A不正确;
B、NH3·H2O显碱性,NaCl显中性,HNO3显酸性,则溶液pH值由高到低: NH3·H2O、NaCl、HNO3,故B不正确;
C、金属活动性顺序由强到弱:Zn、Cu、Ag,故C不正确;
D、Na2S中硫元素质量分数为![]() , Na2SO3中硫元素质量分数为
, Na2SO3中硫元素质量分数为
![]() ,Na2SO4中硫元素质量分数为
,Na2SO4中硫元素质量分数为![]() ,则硫元素质量分数由高到低:Na2S、Na2SO3、Na2SO4,故D正确。故选D。
,则硫元素质量分数由高到低:Na2S、Na2SO3、Na2SO4,故D正确。故选D。

 阅读快车系列答案
阅读快车系列答案【题目】下列用微观粒子观点解释不正确的
现象 | 解释 | |
| 温度计中的水银球受热体积膨胀 | 分子体积受热变大 |
| 宿迁大地,美酒飘香 | 分子在不断运动 |
| 水电解生成氢气和氧气 | 分子可以分为原子 |
| 糖水是混合物 | 糖水有不同种分子 |
A. AB. BC. CD. D
【题目】.研究性学习小组选择“过氧化氢生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
[假 设]过氧化氢生成氧气的快慢与催化剂的种类有关.
[实验方案]常温下,在两瓶同质量、同浓度的过氧化氢溶液中,分别加入相同质量的二氧化锰和水泥块,测量各生成一瓶(相同体积)氧气所需的时间。
[进行实验]
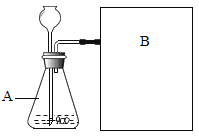
如图是他们进行实验的装置图,气体发生装置中 A 仪器的名称是_______,此实验中 B 处宜采用的气体收集方法是_______ 。
[实验记录]
实验编号 | (1) | (2) |
反应物 | 5%过氧化氢 | 5%过氧化氢 |
催化剂 | 1g水泥块 | 1g二氧化锰 |
时间 | 165秒 | 46秒 |
[结 论]该探究过程得出的结论是_______。
[反 思]
(1)过氧化氢在常温下分解缓慢,若要证明二氧化锰和水泥块是该反应的催化剂,还需增加实验来验证它们在化学反应前后的_______和_______是否改变。
(2)过氧化氢生成氧气的快慢还与哪些因素有关?请你帮助他们继续探究。(只要求提出一种影响过氧化氢生成氧气的快慢因素以及相关假设和实验方案)
[假 设]_______ 。
[实验方案]_______ 。
①用高锰酸钾制取氧气的反应的符号表达式是_______ ,基本反应类型_______



