题目内容
【题目】草酸存在于自然界的植物中。草酸晶体( H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。草酸能与氢氧化钙反应生成沉淀。请回答下列问题:

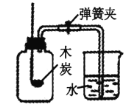
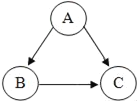
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,仪器a的名称是___。
装置B的主要作用是___。装置C中有气泡逸出,澄清石灰水变浑浊,由此可知草酸晶体分解的产物中一定有___。
(2)乙组同学认为草酸晶体分解的产物中还有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置( 可以重复选用)进行实验。(氢氧化钠溶液能吸收CO2,浓硫酸能吸水)
①乙组同学的实验装置依次连接的合理顺序为:A→B→(__)→(___)→(___)→I→D→H.H装置的作用是___。
②如果有CO气体,则装置I中盛有的氧化铁颜色由___变为___,反应的方程式为___。欲证明草酸晶体分解的产物中有CO,乙组同学需要两次使用装置D,第一次使用现象是___、第二次使用现象是___。
【答案】酒精灯 冷却草酸蒸气,防止与澄清石灰水反应生成白色沉淀,干扰二氧化碳的检验 二氧化碳 F D G 收集尾气 红棕色 黑色 3CO+Fe2O3![]() 2Fe+3CO2 澄清石灰水不变浑浊 澄清石灰水变浑浊。
2Fe+3CO2 澄清石灰水不变浑浊 澄清石灰水变浑浊。
【解析】
(1)仪器a为加热仪器,名称是酒精灯;装置B的主要作用是防止升华的草酸进入C中,与澄清石灰水反应生成白色沉淀,影响CO2的检验;澄清石灰水遇到二氧化碳变浑浊,故说明草酸分解的产物中有二氧化碳气体生成;
(2)①装置AB中生成气体要先经过浓氢氧化钠溶液F吸收二氧化碳,而后经过澄清石灰水D检验二氧化碳是否被完全吸收,然后再经过浓硫酸G除水,后通入到I装置还原氧化铁,经过澄清石灰水检验有二氧化碳生成,故填F、D、G,一氧化碳不溶于水,H的作用为收集过量的一氧化碳尾气。②如果有一氧化碳气体,可观察到的现象是直玻璃管中红棕色粉末逐渐变成黑色,反应的化学方程式是Fe2O3+3CO![]() 2Fe+3CO2,证明草酸晶体分解的产物中有一氧化碳,则第一个D装置中的澄清石灰水应该不变浑浊,二氧化碳已经被氢氧化钠溶液完全吸收,第二个澄清石灰水装置应该变浑浊,是氧化铁与一氧化碳反应生成了二氧化碳。
2Fe+3CO2,证明草酸晶体分解的产物中有一氧化碳,则第一个D装置中的澄清石灰水应该不变浑浊,二氧化碳已经被氢氧化钠溶液完全吸收,第二个澄清石灰水装置应该变浑浊,是氧化铁与一氧化碳反应生成了二氧化碳。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____________。
【查阅资料】CaC12 滚液显中性
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想I:只有CaC12 猜想II:有__________
猜想III:有CaC12和Ca(OH)2 猜想IV:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_________________。
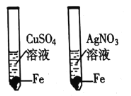
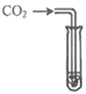
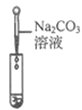
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ____________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
【得出结论】通过探究,全班同学一致确定猜想III是正确的。
【评价反思】(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_______。
【题目】元素周期表和化学用语都是学习化学的重要工具,回答下列问题
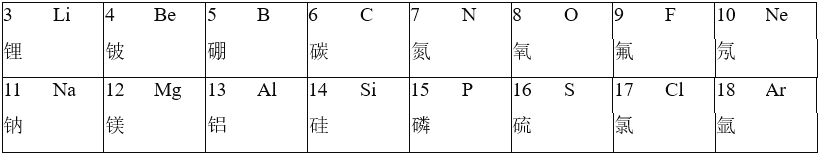
(1)第9号元素的气体单质(该物质的一个分子由两个原子构成)常温下与水发生反应,生成氢氟酸(HF)和另一种具有助燃性的常见气体单质,该反应的化学方程式为_____
(2)中和反应在生产生活中应用广泛
①含有第3号元素的碱,其化学式为_____,其溶液因为含有_____(填微粒符号)而具有碱性,H2SiO3属于_____(填物质类别),推测这两种物质间发生反应的化学方程式为_____
②氢氧化钾溶液与稀硫酸发生反应的化学方程式为_____,恰好完全反应后的溶液因存在_____(填微粒符号)而具有导电性.
③下表是某酸碱指示剂在不同的pH值范围内显示的颜色
颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
pH范围 | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
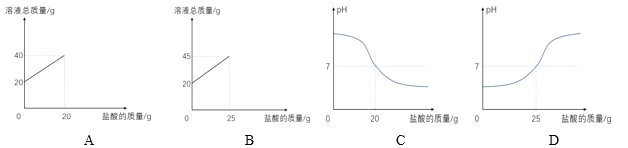
某同学用10%的氢氧化钠溶液、7.3%的稀盐酸和上述指示剂做中和反应的实验,当观察到烧杯中颜色恰好由蓝变绿时氢氧化钠溶液反应消耗了20g,则下列图像正确的是_____(填序号)