题目内容
【题目】请依据下列装置回答问题:

(1)写出标号①的仪器名称_____。
(2)要制取并收集到干燥的氧气。用KClO3和MnO2混合制O2发生装置可选用_____(填装置序号),用装置C干燥O2,气体由导管______(填 “a”或“b”)端进入,收集装置应选用______(填装置序号)。在没有MnO2时可用KMnO4替代MnO2,理由是______,此时应该对发生装置进行一个小改进,具体做法是______。
(3)若用B、F组合成套装 置,请写出一个用该装置制取气体的化学方程式_____。
【答案】长颈漏斗 A a D KMnO4受热分解可以产生MnO2 在试管口内侧放一团棉花 Zn+H2SO4=ZnSO4+H2↑或2H2O2![]() 2H2O+O2↑
2H2O+O2↑
【解析】
(1)标号①的仪器名称是长颈漏斗。
(2)用KClO3和MnO2混合制氧气需要加热,发生装置是固固加热装置,可选用A;可用浓硫酸干燥氧气,选用装置C时,气体从长管进入,从短管排出,故由导管a端进入;氧气密度比空气大,收集装置干燥氧气应选用D;高锰酸钾受热分解能够生成二氧化锰,二氧化锰可以用作催化剂,此时应该对发生装置进行一个小改进,具体做法是在试管口塞一团棉花,以防止加热时高锰酸钾进入导管。
(3)B装置是固液不加热装置,F为排水法收集气体,收集的气体不能溶于水会与水反应。过氧化氢在二氧化锰的催化作用下,分解生成水和氧气,反应方程式为2H2O2![]() 2H2O+O2↑,氧气的密度比空气的密度大,不易溶于水,可用此装置组合制取氧气。通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,氢气难溶于水,密度比空气小,可用此装置组合制取氢气。
2H2O+O2↑,氧气的密度比空气的密度大,不易溶于水,可用此装置组合制取氧气。通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,氢气难溶于水,密度比空气小,可用此装置组合制取氢气。

【题目】为探究某塑料的元素组成,某实验小组设计了实验I和Ⅱ。回答下列问题:
I.制取氧气
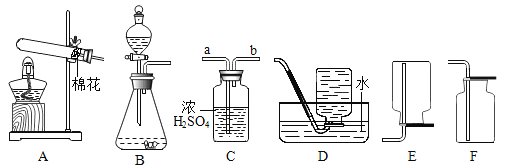
(1)A中用于加热的仪器名称是_______________;若用一种暗紫色固体制取干燥的O2,发生反应的化学方程式为____________,选择的装置组合为__________ (填字母)。
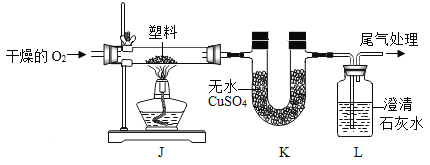
Ⅱ.组成探究
(2)定性检测(已知:无水CuSO4遇水变蓝色)
实验操作 | 实验现象 | 结论 |
连接装置,检查气密性,装入试剂并按上图进行实验。通入干燥的O2,一段时间后,点燃J处酒精灯 | ①装置K中无水CuSO4变__色 | 塑料燃烧产物中有H2O |
②装置L中__________ | 塑料燃烧产物中有CO2 |
③由上述实验可知,该塑料一定含有的元素是___________(填元素符号)。
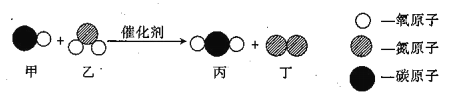
【题目】一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如下图所示。下列说法正确的是( )
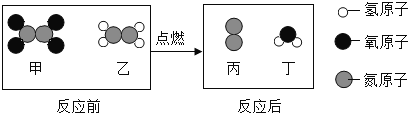
A.甲的化学式为NO2B.乙的相对分子质量为34
C.乙和丙组成元素相同D.生成21g丙的同时生成18g丁
【题目】同学们在做铝与硫酸铜溶液反应的实验时,有的组铜较快析出形成铜树,有的组却较慢。课后,化学小组同学对影响铝与硫酸铜溶液反应速率的因素进行了如下探究。
![]()
(进行实验)如图所示进行实验。小组同学做了实验1和实验2两组实验,实验记录如下表。每次实验中所用铝条长度、粗细相同,伸入到硫酸铜溶液部分绕成的螺旋数相同;硫酸铜溶液的体积相同。
实验1:
编号 | 温度/℃ | 硫酸铜溶液的 溶质质量分数 | 铝条 是否打磨 | 实验现象 |
1-1 | 20℃ | 8% | 打磨 | 生成红色铜树的速度较慢 |
1-2 | 30℃ | 8% | 打磨 | 生成红色铜树的速度较快 |
1-3 | 40℃ | 8% | 打磨 | 生成红色铜树的速度快 |
实验2:
编号 | 温度/℃ | 硫酸铜溶液的 溶质质量分数 | 铝条 是否打磨 | 实验现象 |
2-1 | 20℃ | 16% | 打磨 | 生成红色铜树的速度较快 |
2-2 | 20 | 16% | 未打磨 | 生成红色铜树的速度较慢 |
(解释与结论)
(1)铝与硫酸铜溶液反应的化学方程式为_____。
(2)通过实验1可得到的结论是_____。
(3)通过对比实验_____(填编号),可得到“硫酸铜溶液的溶质质量分数是影响铝与硫酸铜溶液反应速率的因素之一”。
(4)实验2的目的是_____。
(反思与评价)
(5)在做铝与酸反应、铝与盐溶液反应的实验前,要打磨铝条,其目的是除去铝表面的_____(填化学式)。
(6)影响铝与硫酸铜溶液反应速率的因素还可能有_____(写出1条即可)。