题目内容
【题目】自来水厂常用氯气杀菌消毒,用明矾、氯化铁等净化水。以硫铁矿(主要成分是FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的流程如下图所示:
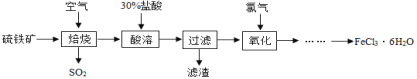
(1)“焙烧”前将硫铁矿进行粉碎,其目的是___。
(2)已知“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,写出该反应的化学方程式__。
(3)大量排放出SO2能形成酸雨,危害环境。常用下列方法除去:
方法1:将含SO2的废气通入氨水中,以减少空气污染,反应的化学方程式为:2SO2+4NH3H2O+O2=2__+2H2O。某兴趣小组测定了不同溶质质量分数的氨水在不同温度下吸收SO2气体的情况,获得如下图象,从实验数据可知,吸收SO2最佳的生产条件是__、__;

方法2:将含有二氧化硫的废气通入石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫。写出该反应的化学方程式____。
(4)流程中用30%盐酸“酸溶”焙烧后的残渣,写出化学方程式____;若在实验室欲用质量分数为37%(密度为1.18 g/ml)的盐酸配制30%的100g盐酸,则需要加水___g(保留1位小数),需要的玻璃仪器有烧杯、___、___胶头滴管等。
(5)“氧化”后从FeCl3溶液中获得FeCl3·6H2O晶体的操作方法是:在HCl气流中蒸发浓缩、____、过滤、洗涤、干燥。
【答案】增大接触面积,加快反应 4FeS2+11O2![]() 2Fe2O3+8SO2 (NH4)2SO4 2%的氨水 50℃ 2CaCO3+2SO2+O2=2CaSO4+2CO2 Fe2O3+6HCl=2FeCl3 +3H2O 18.9 量筒 玻璃棒 降温结晶
2Fe2O3+8SO2 (NH4)2SO4 2%的氨水 50℃ 2CaCO3+2SO2+O2=2CaSO4+2CO2 Fe2O3+6HCl=2FeCl3 +3H2O 18.9 量筒 玻璃棒 降温结晶
【解析】
硫铁矿和氧气在点燃条件下生成氧化铁和二氧化硫,增大反应物的接触面积可以加快反应速率,二氧化硫和氨水和氧气生成硫酸铵和水,二氧化硫通入灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,氧化铁和盐酸反应生成氯化铁和水。
(1)“焙烧”前将硫铁矿进行粉碎,其目的是增大接触面积,加快反应。
(2)“焙烧”阶段就是硫铁矿的燃烧,生成物是Fe2O3和SO2,反应的化学方程式为
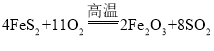 。
。
(3) 方法1:将含SO2的废气通入氨水中,通入空气生成硫酸铵和水,吸收二氧化硫,反应的化学方程式为:![]() 。测定了不同溶质质量分数的氨水在不同温度下吸收SO2气体的情况,获得如下图象,从实验数据可知,吸收
。测定了不同溶质质量分数的氨水在不同温度下吸收SO2气体的情况,获得如下图象,从实验数据可知,吸收
![]() 最佳的生产条件是2%的氨水、50℃。
最佳的生产条件是2%的氨水、50℃。
方法2:将含有二氧化硫的废气通入石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫。反应的化学方程为![]() 。
。
(4)流程中用30%盐酸“酸溶”焙烧后的残渣,盐酸和氧化铁反应生成氯化铁和水,化学方程式为![]() ;若在实验室欲用质量分数为37%(密度为1.18 g/ml)的盐酸配制30%的100g盐酸,则需要加水
;若在实验室欲用质量分数为37%(密度为1.18 g/ml)的盐酸配制30%的100g盐酸,则需要加水![]() ,需要的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管等。
,需要的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管等。
(5)“氧化”后从FeCl3溶液中获得FeCl3·6H2O晶体的操作方法是:在HCl气流中蒸发浓缩、降温结晶、过滤、洗涤、干燥。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】某小组同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如图1所示(已知氯化钙溶液呈中性;石灰石中的杂质不与酸反应,也不溶于水)。
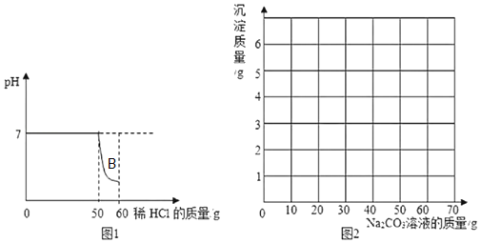
①图1中B点溶液中的溶质有_____(写化学式)。
②该小组同学能收集到的二氧化碳的质量是_____g,同时可得到CaCl2的质量为_____g。
③该小组同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m=_____。加入10gNa2CO3溶液时发生反应的化学方程式是_____。
④请在图2中画出向滤液中加入Na2CO3溶液时产生的沉淀的质量随加入Na2CO3溶液的变化曲线_____。
【题目】依据下列20℃时的实验和数据回答以下问题。
已知:20℃时,KCl和KNO3的溶解度分别为34g和31.6g;
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | KCl | KCl | KCl | KNO3 | KNO3 | |
固体的质量/g | 20 | 35 | 40 | 25 | 40 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
【1】①~⑤所得溶液属于不饱和溶液的是
A. ①②B. ②③C. ①④D. ③⑤
【2】下列关于①~⑤所得溶液的说法正确的是
A. 溶质质量:③ = ⑤
B. 溶液质量:③﹥②
C. 溶质质量分数:①<④
D. ⑤中溶质与溶剂的质量比为2:5