题目内容
【题目】(6分)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁,他们为了测定水垢中碳酸钙的含量,取某种稀盐酸100 g加入到15.8 g水垢中,产生CO2气体的情况如下图所示。计算:
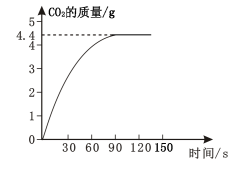
(1)从图中可以看出15.8 g水垢与盐酸反应后生成CO2最多是 。
(2)水垢中碳酸钙的质量分数是多少?(计算结果保留0.1%)
(3)所用稀盐酸中溶质质量分数是多少?(计算结果保留0.1%)
【答案】(1)4.4g;(2)63.3%;(3)7.3%
【解析】
试题分析:盐酸中溶质的质量由表中数据可以判断生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量、稀盐酸中氯化氢的质量,进一步可以计算水垢中碳酸钙的质量分数和所用稀分数.
(1)从图中可以看出15.8g水垢与盐酸反应后生成CO2最多是4.4g.
(2)设碳酸钙的质量为x,氯化氢的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 4.4g
![]() =
=![]() =
=![]() ,
,
x=10g,y=7.3g,
水垢中碳酸钙的质量分数是:![]() ×100%=63.3%,
×100%=63.3%,
答:水垢中碳酸钙的质量分数是63.3%.
(3)所用稀盐酸中溶质质量分数是:![]() ×100%=7.3%,
×100%=7.3%,
答:所用稀盐酸中溶质质量分数是7.3%.

练习册系列答案
相关题目