题目内容
【题目】鸡蛋壳的主要成分是碳酸钙,其余为杂质,(杂质不溶于水且不参加反应)为了测定蛋壳中碳酸钙的质量分数。小东和小明同学进行了如下实验,相关实验数据如下图所示:
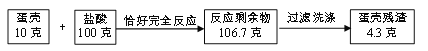
(1)小东根据“蛋壳残渣质量为4.3克”,求得蛋壳中碳酸钙的质量分数为_________;
(2)小明根据“反应过程中减少的质量”(10克+100克-106.7克=3.3克)也求得了蛋壳中碳酸钙的质量分数,请你写出小明的计算过程和结果__________________。
(3)小东和小明经过反复实验得出该鸡蛋壳中碳酸钙的质量分数与小明结果吻合,请分析小东开始所得结果出现误差的原因是__________________________。
【答案】 57% 75% 小东计算所用的蛋壳残渣未干燥
【解析】(1)小东根据“蛋壳残渣质量为4.3克”,求得蛋壳中碳酸钙的质量分数为(10g-4.3g)÷10g×100%=57%;(2)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,所以生成二氧化碳的质量=参加反应前各物质的质量总和反应后剩余各物质的质量总和;生成二氧化碳的质量为:10g+100g-106.7g=3.3g;
设:碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
10044
x3.3g
100/x=44/3.3g x=7.5g,
蛋壳中碳酸钙的质量分数: 7.5g÷10g×100%=75%;
(3)小东开始所得结果出现误差的原因是小东计算所用的蛋壳残渣未干燥。使滤渣的质量偏高。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目