题目内容
(6分)小强在家庭装修的废弃料中看到一些大理石碎料,他想探究大理石中碳酸钙的含量。于是他取部分大理石带到实验室,砸碎后称取25g,加入200g稀盐酸恰好完全反应,测得生成二氧化碳的质量为8.8g。
求:⑴大理石中碳酸钙的质量分数。
⑵所用稀盐酸的溶质质量分数。
求:⑴大理石中碳酸钙的质量分数。
⑵所用稀盐酸的溶质质量分数。

分析:(1)大理石中碳酸钙的质量分数=  ×100%,
×100%,
所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的碳酸钙的质量,即样品中所含碳酸钙的质量;
(2)所用稀盐酸的溶质质量分数= ×100%,所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的HCl的质量,即200g稀盐酸中所含HCl的质量.
×100%,所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的HCl的质量,即200g稀盐酸中所含HCl的质量.
解:设25g大理石样品中含碳酸钙的质量为x,所用盐酸中溶质的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 8.8g
 =
=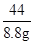
x=20g
大理石中碳酸钙的质量分数=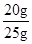 ×100%=80%
×100%=80%
 =
=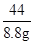
y=14.6g
稀盐酸的溶质质量分数=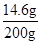 ×100%=7.3%
×100%=7.3%
答::(1)大理石中碳酸钙的质量分数为80%;
(2)所用稀盐酸的溶质质量分数为7.3%.
点评:恰好完全反应即大理石中的碳酸钙和稀盐酸中溶质氯化氢都全部反应
 ×100%,
×100%,所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的碳酸钙的质量,即样品中所含碳酸钙的质量;
(2)所用稀盐酸的溶质质量分数=
 ×100%,所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的HCl的质量,即200g稀盐酸中所含HCl的质量.
×100%,所以,需要利用反应的化学方程式根据生成二氧化碳气体的质量计算出参加反应的HCl的质量,即200g稀盐酸中所含HCl的质量.解:设25g大理石样品中含碳酸钙的质量为x,所用盐酸中溶质的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 8.8g
 =
=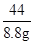
x=20g
大理石中碳酸钙的质量分数=
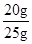 ×100%=80%
×100%=80% =
=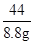
y=14.6g
稀盐酸的溶质质量分数=
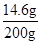 ×100%=7.3%
×100%=7.3%答::(1)大理石中碳酸钙的质量分数为80%;
(2)所用稀盐酸的溶质质量分数为7.3%.
点评:恰好完全反应即大理石中的碳酸钙和稀盐酸中溶质氯化氢都全部反应

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
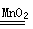 2 H2 O+O2↑从化学反应的基本类型来看,它们都属于 反应。
2 H2 O+O2↑从化学反应的基本类型来看,它们都属于 反应。