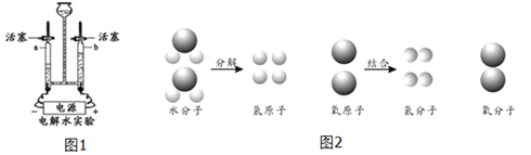��Ŀ����
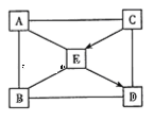
����Ŀ����������װ��ͼ���ش��й����⣺
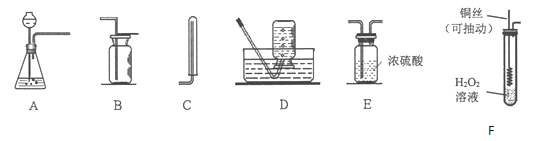
��1��ʵ�����ù���������ȡ�����Ļ�ѧ����ʽΪ ����Ҫ��ȡ���ռ�һƿ�����������Ӧѡ��װ�õ�����˳��Ϊ ��ѡ����ĸ�������������Ƿ��ռ����ķ���Ϊ ��
��2��ʵ���ҳ���п����ϡ���ᷴӦ��ȡ�������йط�Ӧ�Ļ�ѧ����ʽΪ �������ſ������ռ���Ӧѡ�õ��ռ�װ��Ϊ ��ѡ����ĸ����
��3��ʵ��Ľ����������Ϸ��֣�����ͭ����������������ֽ��������Ĵ���������һ���ྻ��ͭ˿��ʵ��ǰ�Ƚ����Ƴ�����״���پ��� �������Ľ���ķ���װ����ͼF��ʾ������ȥ�г�װ������
��ͭ˿�Ƴ�����״��������
A���ռ��������O2 B���ӿ췴Ӧ���� C��û��Ӱ��
����װ��A�Ƚϣ��Ľ���װ�õ��ŵ��� ��
���𰸡���1��2H2O2![]() 2H2O+O2����A��E��B����һ�������ǵ�ľ�����ڼ���ƿ�ڣ�
2H2O+O2����A��E��B����һ�������ǵ�ľ�����ڼ���ƿ�ڣ�
��2��Zn+H2SO4=ZnSO4+H2����C��
��3������ B ����ʱ���Ʒ�Ӧ�Ľ���
��������
���������
��1�����������ڶ������̵Ĵ������·ֽ�Ϊˮ����������Ϊ��Ӧ���ǹ�����Һ�壬�ڳ����½��У�ѡ��װ��A����ȡ���ռ�һƿ�������������Ũ���������и���������ſ��������ռ�����������ʱ���ɽ�һ�������ǵ�ľ�����ڼ���ƿ�ڣ��۲�ľ���Ƿ�ȼ��
��2��п��ϡ���ᷴӦ��������п����������Ϊ�������ܶȱȿ���С�����Կ��������ſ��������ռ���
��3����ͭ˿���գ�ͭ��������Ӧ��������ͭ��
�ٽ�ͭ˿�Ƴ�����״���������뷴Ӧ��ĽӴ�������ӿ��˷�Ӧ�����ʣ�
���������⣬��������Ӵ����������̺�Ӧ��������ʼ��������Ϊ���������ʺ������������������Ľ����װ�ã�ͨ���鶯ͭ˿�����Ʒ�Ӧ�ķ�����ֹͣ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�