题目内容
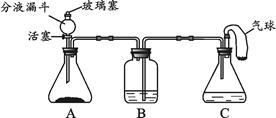
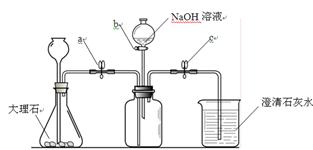
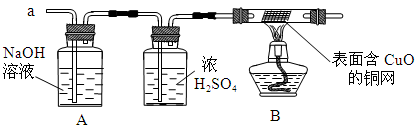
(5分)利用化学反应中气体产生的压力,可使多个化学反应依次发生,根据图示回答下列问题(A装置中的试剂足量,B、C、D中的试剂少量):
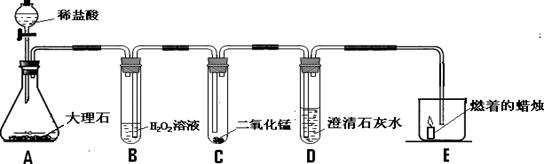
(1)打开A中分液漏斗的活塞,使稀盐酸逐滴滴下,A中的反应方程式是 。
(2)B中观察到的现象是 。
(3)C中开始和后来观察到的现象是 。
(4)D中发生反应的方程式 。
(5)E中的现象是 。

(1)打开A中分液漏斗的活塞,使稀盐酸逐滴滴下,A中的反应方程式是 。
(2)B中观察到的现象是 。
(3)C中开始和后来观察到的现象是 。
(4)D中发生反应的方程式 。
(5)E中的现象是 。
(1)CaCO3+2HCl==CaCl2+CO2↑+H2O
(2)试管内液体沿导管流出
(3)开始从导管流入的液体遇黑色粉末产生气泡,后来产生的气泡越来越少,从导管内有气泡冒出。
(4)CO2+ Ca(OH)2 ="=" CaCO3↓+H2O
(5)蜡烛先明亮后熄灭
(2)试管内液体沿导管流出
(3)开始从导管流入的液体遇黑色粉末产生气泡,后来产生的气泡越来越少,从导管内有气泡冒出。
(4)CO2+ Ca(OH)2 ="=" CaCO3↓+H2O
(5)蜡烛先明亮后熄灭
试题分析:(1)据图可知,A中的反应物是稀盐酸和大理石,反应生成氯化钙、水和二氧化碳,故反应的化学反应式为CaCO3+2HCl═CaCl2+CO2↑+H2O。
(2)A中生成的二氧化碳气体进入B,使B中的压强增大,在气压的作用下,B中的H2O2溶液会沿导管进入C。
(3)进入C的H2O2溶液在二氧化锰的催化作用下,会迅速反应生成氧气,所以开始可以看到流入的液体遇黑色粉末即产生气泡,且越来越多;但由于B中试剂少量,故待双氧水反应完后,就不再有气泡产生,这时会有来自B的二氧化碳气体(A装置中的试剂足量)从导管内冒出,故可见导管内有气泡冒出。
(4)A、C中生成的气体都会进入D,其中A中生成的二氧化碳气体可以使澄清的石灰水变浑浊,化学反应式是:CO2+Ca(OH)2═CaCO3↓+H2O。
(5)由于C中产生的氧气先进入E,而氧气有助燃性,故可见蜡烛火焰变得更明亮,但由于B中试剂少量,故待双氧水反应完后,就不再有氧气产生;而这时由于A装置中的试剂足量,会不断产生二氧化碳气体,且由于D中的试剂少量,所以二氧化碳气体并没有全部反应,会有大量的二氧化碳剩余,并沿导管进入E,由于二氧化碳不可燃,也不支持燃烧,所以进入E的二氧化碳气体会使蜡烛熄灭。
点评:熟练掌握氧气和二氧化碳的实验室制法及反应原理,了解常见气体的性质,并能正确书写化学方程式,是解答本题的关键;所以要求同学们在平时的学习中要加强基础知识的储备,以便能够灵活应用。

练习册系列答案
相关题目
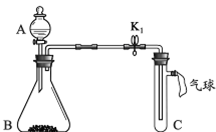
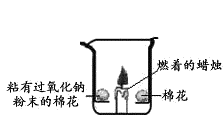
 (燃烧匙中的药品为红磷)
(燃烧匙中的药品为红磷)