题目内容
(2008?西城区一模)水是生命之源,自然界中的水经过不同处理后,用途更加广泛.
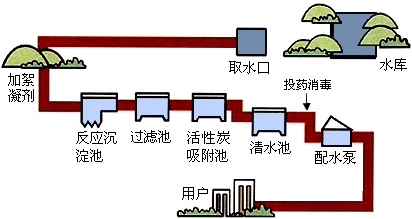
(1)如图是自来水厂的净水过程,其中除去水中不溶性杂质的主要设备是
(2)目前,许多自来水厂采用氯气进行杀菌消毒.常温下,氯气能与水反应生成盐酸和次氯酸(HClO),次氯酸能杀菌消毒.
①氯气与水反应的化学方程式为
②若用自来水(密度视为1g/cm3)配制溶质质量分数为1%的下列溶液,溶质的质量分数不受影响的是
A.稀盐酸 B.碳酸钠溶液 C.氢氧化钠溶液 D.硝酸钾溶液.

(1)如图是自来水厂的净水过程,其中除去水中不溶性杂质的主要设备是
过滤
过滤
池,除去臭味和一些可溶性杂质的设备是活性炭吸附
活性炭吸附
池.经过以上处理的自来水不是纯水,若要制取纯水,应采取的净化方法是蒸馏
蒸馏
.(2)目前,许多自来水厂采用氯气进行杀菌消毒.常温下,氯气能与水反应生成盐酸和次氯酸(HClO),次氯酸能杀菌消毒.
①氯气与水反应的化学方程式为
Cl2+H2O═HCl+HClO
Cl2+H2O═HCl+HClO
.②若用自来水(密度视为1g/cm3)配制溶质质量分数为1%的下列溶液,溶质的质量分数不受影响的是
D
D
(填序号).A.稀盐酸 B.碳酸钠溶液 C.氢氧化钠溶液 D.硝酸钾溶液.
分析:(1)过滤能除去水中的不溶性固体;活性炭有吸附作用,可除去水中部分可溶性杂质、异味和色素;蒸馏获得的是蒸馏水,不含有其它的杂质,制得的是纯水.
(2)①由题意,氯气能与水反应生成盐酸和次氯酸(HClO),写出反应的化学方程式即可.
②根据题意,自来水中含有盐酸和次氯酸(HClO),因此在使用自来水配制溶液时,自来水中的盐酸和次氯酸可能会与加入的固体溶质发生反应,而使所配制的溶液不能达到配制要求;故使用自来水配制溶液,溶质质量分数不受影响的应该是溶质不能自来水中盐酸等发生反应的物质.
(2)①由题意,氯气能与水反应生成盐酸和次氯酸(HClO),写出反应的化学方程式即可.
②根据题意,自来水中含有盐酸和次氯酸(HClO),因此在使用自来水配制溶液时,自来水中的盐酸和次氯酸可能会与加入的固体溶质发生反应,而使所配制的溶液不能达到配制要求;故使用自来水配制溶液,溶质质量分数不受影响的应该是溶质不能自来水中盐酸等发生反应的物质.
解答:解:(1)过滤能除去水中的不溶性固体,故除去水中不溶性杂质的主要设备是过滤池;活性炭有吸附作用,可除去水中部分可溶性杂质、异味和色素,故除去臭味和一些可溶性杂质的设备是活性炭吸附池;制取纯水的方法主要通过蒸馏的方法.
(2)①氯气与水反应生成盐酸和次氯酸(HClO),反应的化学方程式为Cl2+H2O═HCl+HClO.
②解:A、由于自来水中含有盐酸,故使用自来水配制的稀盐酸会因自来水中含的盐酸的影响,而大于所要配制的1%.
B、由于碳酸钠会与自来水中的盐酸、次氯酸发生反应而减少,故使用自来水配制的碳酸钠溶液的质量分数小于所要配制的1%.
C、由于氢氧化钠会与自来水中的盐酸、次氯酸发生反应而减少,故使用自来水配制的氢氧化钠溶液的质量分数小于所要配制的1%.
D、由于硝酸钾不能与自来水中的盐酸、次氯酸等发生反应,故使用自来水配制的硝酸钾溶液的质量分数不会受到自来水中物质的影响.
故选D.
故答案为:(1)过滤;活性炭吸附;蒸馏;
(2)①Cl2+H2O═HCl+HClO;②D.
(2)①氯气与水反应生成盐酸和次氯酸(HClO),反应的化学方程式为Cl2+H2O═HCl+HClO.
②解:A、由于自来水中含有盐酸,故使用自来水配制的稀盐酸会因自来水中含的盐酸的影响,而大于所要配制的1%.
B、由于碳酸钠会与自来水中的盐酸、次氯酸发生反应而减少,故使用自来水配制的碳酸钠溶液的质量分数小于所要配制的1%.
C、由于氢氧化钠会与自来水中的盐酸、次氯酸发生反应而减少,故使用自来水配制的氢氧化钠溶液的质量分数小于所要配制的1%.
D、由于硝酸钾不能与自来水中的盐酸、次氯酸等发生反应,故使用自来水配制的硝酸钾溶液的质量分数不会受到自来水中物质的影响.
故选D.
故答案为:(1)过滤;活性炭吸附;蒸馏;
(2)①Cl2+H2O═HCl+HClO;②D.
点评:本题难度不大,掌握自来水厂的净水的知识、酸的化学性质、化学方程式的书写及灵活运用所学知识等是正确解答本题的关键.

练习册系列答案
相关题目

