题目内容
某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素。实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10 g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1 g/em3;大理石中杂质不与盐酸反应)。
(1)反应原理:实验中的化学方程式 。
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关。
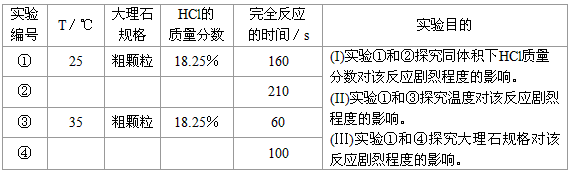
(3)实验设计与实施:完成以下实验设计方案并实验。
(1)反应原理:实验中的化学方程式 。
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关。
(3)实验设计与实施:完成以下实验设计方案并实验。
(4)实验结论: 。
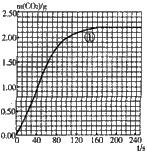
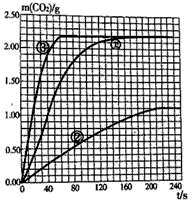
(5)绘制图像:实验①中CO2质量随时问变化的关系如下图,借助简单计算请在右图中画出实验②和③中
CO2质量随时间变化关系的曲线(忽略溶液体积变化)。说明:可以用铅笔画曲线。
(5)绘制图像:实验①中CO2质量随时问变化的关系如下图,借助简单计算请在右图中画出实验②和③中
CO2质量随时间变化关系的曲线(忽略溶液体积变化)。说明:可以用铅笔画曲线。
(1) 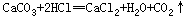
(3)
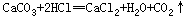
(3)

(4)在其他条件不变时,盐酸质量分数越大,反应越剧烈;温度越高,反应越剧烈;固体的颗粒越小,反应越剧烈。
(5)作图要点:实验②的曲线,纵坐标对应的每一个值均为实验①的1/2,在210s时是直线。实验③的曲线,升高温度,反应剧烈程度增大,产生二氧化碳的量不变,所以图像曲线低利率变大,在60s时与实验①高度相同。
(5)作图要点:实验②的曲线,纵坐标对应的每一个值均为实验①的1/2,在210s时是直线。实验③的曲线,升高温度,反应剧烈程度增大,产生二氧化碳的量不变,所以图像曲线低利率变大,在60s时与实验①高度相同。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/em3;大理石中杂质不与盐酸反应).
(1)反应原理:实验中的化学方程式 .
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:完成以下实验设计方案并实
(4)实验结论: .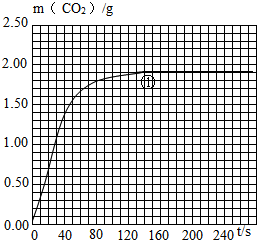
(5)绘制图象:实验①中CO2质量随时问变化的关系如图,借助简单计算请在右图中画出实验②和③中CO2质量随时间变化关系的曲线(忽略溶液体积变化).
说明:可以用铅笔画曲线.
(1)反应原理:实验中的化学方程式
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:完成以下实验设计方案并实
| 实验编号 | T/℃ | 大理石 规格 |
HCl的质量分数 | 完全反应的 时间/s |
实验目的 |
| ① | 25 | 粗颗粒 | 18.25% | 160 | (Ⅰ)实验①和②探究同体积下HCl的质量分数对该反应剧烈程度的影响. (Ⅱ)实验①和③探究温度对该反应剧烈程度的影响. (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响. |
| ② | 210 | ||||
| ③ | 35 | 粗颗粒 | 18.25% | 60 | |
| ④ | 100 |

(5)绘制图象:实验①中CO2质量随时问变化的关系如图,借助简单计算请在右图中画出实验②和③中CO2质量随时间变化关系的曲线(忽略溶液体积变化).
说明:可以用铅笔画曲线.
某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为10%、20%,每次实验HCl的用量为20mL.(假设10%、20%的盐酸的密度均为1g/cm3;大理石中杂质不与盐酸反应)
(1)反应原理:实验中的化学方程式______.
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:根据实验目的完成以下实验设计方案并实验.
(4)实验结论:______.
(1)反应原理:实验中的化学方程式______.
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:根据实验目的完成以下实验设计方案并实验.
| 实验 编号 | 温度/℃ | 大理石 规格 | HCl的质量分数 | 完全反应的时间/s | 实验目的 |
| ① | 25 | 粗颗粒 | 20% | 160 | (I)实验①和②探究同体积下HCl质量分数对该反应剧烈程度的影响. (II)实验①和③探究温度对该反应剧烈程度的影响. (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响. |
| ② | 210 | ||||
| ③ | 35 | 粗颗粒 | 20% | 60 | |
| ④ | 100 |
25.(2009?潍坊)某化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素.实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10g;所用HCl的质量分数为9.125%、18.25%,每次实验HCl的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1g/em3;大理石中杂质不与盐酸反应).
(1)反应原理:实验中的化学方程式______.
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:完成以下实验设计方案并实
(4)实验结论:______.
(5)绘制图象:实验①中CO2质量随时问变化的关系如图,借助简单计算请在右图中画出实验②和③中CO2质量随时间变化关系的曲线(忽略溶液体积变化).
说明:可以用铅笔画曲线.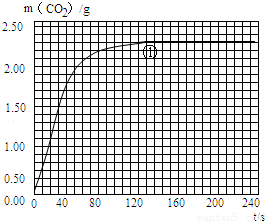
(1)反应原理:实验中的化学方程式______.
(2)提出假设:HCl与大理石反应的剧烈程度与所用HCl的质量分数、大理石规格、反应温度有关.
(3)实验设计与实施:完成以下实验设计方案并实
| 实验编号 | T/℃ | 大理石 规格 | HCl的质量分数 | 完全反应的 时间/s | 实验目的 |
| ① | 25 | 粗颗粒 | 18.25% | 160 | (Ⅰ)实验①和②探究同体积下HCl的质量分数对该反应剧烈程度的影响. (Ⅱ)实验①和③探究温度对该反应剧烈程度的影响. (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响. |
| ② | ______ | ______ | ______ | 210 | |
| ③ | 35 | 粗颗粒 | 18.25% | 60 | |
| ④ | ______ | ______ | ______ | 100 |
(5)绘制图象:实验①中CO2质量随时问变化的关系如图,借助简单计算请在右图中画出实验②和③中CO2质量随时间变化关系的曲线(忽略溶液体积变化).
说明:可以用铅笔画曲线.
