题目内容
【题目】将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,并根据观察到的现象绘制了如图曲线,根据图示回答问题: 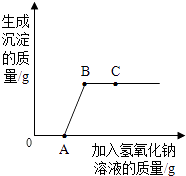
(1)A点处溶液的溶质是;
(2)请写出AB段发生反应的化学方程式;
(3)C点处溶液的pH7(填“>”、“=”或“<”).
【答案】
(1)氯化钠和氯化铜
(2)CuCl2+2NaOH═Cu(OH)2↓+2NaCl
(3)>
【解析】解:将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,氢氧化钠溶液先和盐酸反应生成氯化钠和水,当盐酸反应完后氢氧化钠溶液再和氯化铜反应生成氢氧化铜沉淀和氯化钠.(1)A点没有沉淀生成,说明氢氧化钠溶液只和盐酸反应生成氯化钠和水,而氯化铜还没有反应,所以此处溶液的溶质是氯化钠和氯化铜.故填:氯化钠和氯化铜;(2)AB段是氢氧化钠溶液和氯化铜反应生成氢氧化铜沉淀和氯化钠,发生反应的化学方程式CuCl2+2NaOH═Cu(OH)2↓+2NaCl.故填:CuCl2+2NaOH═Cu(OH)2↓+2NaCl;(3)C点处是氢氧化钠溶液过量,所以此时溶液呈碱性,溶液的pH大于7.故填:>.
【考点精析】利用书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知注意:a、配平 b、条件 c、箭号.

练习册系列答案
相关题目