题目内容
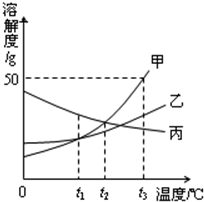 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:(1)t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶液的质量之比为
(2)t2℃时,甲、乙、丙三种物质的饱和溶液中,溶质质量分数的大小关系是
(3)将t3℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液的质量的大小关系是
分析:(1)溶液具有均一性,一定温度下的饱和溶液中溶质、溶剂、溶液的质量比是相同的,可据该温度下甲的溶解度分析解答;
(2)据饱和时质量分数的计算式
×100%可知:溶解度越大质量分数也就越大,并结合溶解度曲线回答;
(3)据三种物质的溶解度受温度影响情况分析判断.
(2)据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(3)据三种物质的溶解度受温度影响情况分析判断.
解答:解:(1)由于溶液具有均一性,所以一定温度下的饱和溶液中溶质、溶剂、溶液的质量比是相同的;t3℃时,甲物质的溶解度是50g,则其饱和溶液中,溶质、溶剂、溶液的质量之比为 50g:100g:150g=1:2:3;
(2)t2℃时,甲、乙、丙三种物质的溶解度大小关系是甲=丙>乙,据饱和时质量分数的计算式
×100%可知:溶解度越大质量分数也就越大,所以该温度下的饱和溶液中,溶质质量分数的大小关系是甲=丙>乙;
(3)由图可知:甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,且温度从t3℃降到t1℃甲的溶解度变化比乙大,所以将t3℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,甲析出晶体的质量大于乙,而丙变为不饱和溶液,溶液的质量不变,则所得溶液的质量的大小关系是丙>乙>甲;
故答案为:(1)1:2:3;(2)甲=丙>乙; (3)丙>乙>甲.
(2)t2℃时,甲、乙、丙三种物质的溶解度大小关系是甲=丙>乙,据饱和时质量分数的计算式
| 溶解度 |
| 溶解度+100g |
(3)由图可知:甲、乙的溶解度随温度的降低而减小,丙的溶解度随温度的降低而增大,且温度从t3℃降到t1℃甲的溶解度变化比乙大,所以将t3℃的甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,甲析出晶体的质量大于乙,而丙变为不饱和溶液,溶液的质量不变,则所得溶液的质量的大小关系是丙>乙>甲;
故答案为:(1)1:2:3;(2)甲=丙>乙; (3)丙>乙>甲.
点评:明确溶解度概念、溶解度曲线的意义,饱和溶液中溶质的质量分数计算方法及等质量的饱和溶液降低相同的温度,溶解度变化大的析出晶体多,才能正确分析解答.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
 (2011?保山)如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法不正确的是( )
(2011?保山)如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法不正确的是( ) 10、如图是甲、乙、丙三种物质的溶解度曲线,则下列有关说法不正确的是( )
10、如图是甲、乙、丙三种物质的溶解度曲线,则下列有关说法不正确的是( ) 5、如图是甲、乙、丙三种物质的溶解度曲线,下面说法不正确的是( )
5、如图是甲、乙、丙三种物质的溶解度曲线,下面说法不正确的是( )

 如图是甲、乙、丙三种固体(均不含结晶水)的溶解度曲线.20℃时,烧杯中分别盛有相同质量的甲、乙、丙饱和溶液,各加入等质量的对应固体,并升温至40℃,观察到,甲固体逐渐减少至全部溶解,下列判断正确的是( )
如图是甲、乙、丙三种固体(均不含结晶水)的溶解度曲线.20℃时,烧杯中分别盛有相同质量的甲、乙、丙饱和溶液,各加入等质量的对应固体,并升温至40℃,观察到,甲固体逐渐减少至全部溶解,下列判断正确的是( )