题目内容
【题目】镁是一种化学性质非常活泼的金属.在点燃或加热的条件下,能跟许多物质发生反应,如:
2Mg+CO2![]() 2MgO+C Mg+2H2O
2MgO+C Mg+2H2O![]() Mg(OH)2+H2↑
Mg(OH)2+H2↑
(1)在点燃的条件下,镁能和氮气反应生成一种淡黄色的固体氮化镁(化学式Mg3N2),氮化镁能和水反应生成一种白色固体,同时放出有刺激性气味的气体.则:
①氮化镁和水反应生成的刺激性气体是 (写化学式).
②检验生成的气体的方法是 .
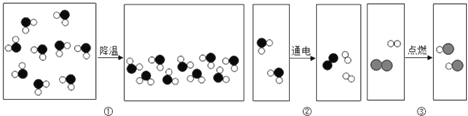
(2)小芳和小刚准备用空气为原料,利用下列装置制取少量氮化镁.请你帮助解决下列问题:
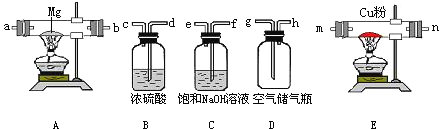
组装装置时导管口的连接顺序 (填导管口序号,每种装置只能用一次).
【答案】(1)①NH3;②把气体通入紫色石蕊试液,溶液变蓝色;
(2)h﹣f﹣e﹣d﹣c﹣m﹣n﹣a﹣b.
【解析】(1)①由题意可知,氮化镁能和水反应生成一种白色固体,同时放出有刺激性气味的气体.由质量守恒定律反应前后元素的种类不变可知:氮化镁和水反应生成的刺激性气体是氨气,化学式是NH3.
②由于氨气极易溶于水,氨水显碱性,检验生成的气体的方法是:把气体通入紫色石蕊试液,溶液变蓝色.
(2)根据题中信息可知,Mg在空气中点燃可以和O2、CO2、H2O反应,所以镁和氮气反应前必须将空气中的O2、CO2、H2O除去制得干燥纯净的N2,应先通过浓氢氧化钠是除去空气中二氧化碳,再通过浓硫酸除去水蒸气,最后通过灼热的铜粉除去空气中氧气即可得到纯净的氮气,氮气与镁反应即可得到氮化镁,所以连接的顺序是h﹣f﹣e﹣d﹣c﹣m﹣n﹣a﹣b.

【题目】某科学兴趣小组在课外活动中,对某无色透明溶液进行了多次检测,其中三次检测结果如表所示,请回答:
检测次数 | 溶液中检测出的物质 |
第一次 | KCl、K2SO4、Na2CO3、NaCl |
第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
第三次 | Na2SO4、KCl、K2CO3、NaCl |
(1)三次检测结果中第 次检测结果不正确.
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,先向溶液中加入过量的稀HNO3溶液;然后继续加入过量的 溶液;过滤后,再向滤液中加入AgNO3溶液.
(3)测得某溶液中仅含有Na+、Mg2+、SO42﹣、Cl﹣四种离子,其中离子个数比为Na+:Mg2+:Cl﹣=4:5:8.若设Na+为4n个,则SO42﹣的离子数为 .