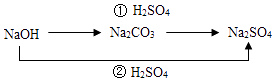题目内容
【题目】某白色粉末中可能含有氧化钙、硫酸钠、氢氧化钠、碳酸钠、氯化钠中的一种或几种物质,为探究他们的成分,某化学小组开展了如图所示的实验. 
回答下列问题:
(1)由步骤Ⅰ可知原白色粉末中一定含有的物质是 . 由步骤Ⅲ得出的结论是 .
(2)根据步骤IV不能确定原白色粉末中某种物质一定存在的理由是 , 要证明该物质的存在,需要对实验进行的改进是 . 原白色粉末中还有一种物质不能确定其是否含有,这种物质是 .
(3)无色溶液C中除了酚酞外一定还含有的溶质是: .
【答案】
(1)氧化钙、碳酸钠;原白色粉末中不含硫酸钠
(2)加入的过量稀盐酸(或步骤Ⅱ中生成的氯化钠)也能与硝酸银溶液反应生成白色沉淀;将步骤Ⅱ中过量的稀盐酸换成过量的稀硝酸;氢氧化钠
(3)Ba(NO3)2、HCl、NaCl
【解析】解:氧化钙和水反应会生成氢氧化钙,氢氧化钙和碳酸钠反应会生成碳酸钙沉淀,碳酸钠和盐酸会生成二氧化碳气体.
白色粉末加水酚酞会生成白色沉淀E和红色溶液A,红色溶液A中加入过量的稀盐酸,会生成无色气体和无色溶液B,所以混合物中一定含有氧化钙和碳酸钠,可能含有氢氧化钠,所以E是碳酸钙沉淀,无色气体是二氧化碳,所以B中一定含有氯化钠,还不能确定混合物中是否存在氯化钠、硫酸钠,需要先检验硫酸钠,所以加入试剂M是硝酸钡,没有明显现象,说明混合物中一定不含硫酸钠,然后检验氯化钠,需要加入硝酸银,会生成氯化银沉淀,所以(1)由步骤Ⅰ可知原白色粉末中一定含有的物质是氧化钙、碳酸钠,由步骤Ⅲ得出的结论是原白色粉末中不含硫酸钠;(2)根据步骤IV不能确定原白色粉末中某种物质一定存在的理由是加入的过量稀盐酸(或步骤Ⅱ中生成的氯化钠)也能与硝酸银溶液反应生成白色沉淀,要证明该物质的存在,需要对实验进行的改进是将步骤Ⅱ中过量的稀盐酸换成过量的稀硝酸.原白色粉末中还有一种物质不能确定其是否含有,这种物质是氢氧化钠.(3)无色溶液C中除了酚酞外一定还含有的溶质是:Ba(NO3)2、HCl、NaCl.
所以答案是:(1)氧化钙、碳酸钠,原白色粉末中不含硫酸钠;(2)加入的过量稀盐酸(或步骤Ⅱ中生成的氯化钠)也能与硝酸银溶液反应生成白色沉淀;将步骤Ⅱ中过量的稀盐酸换成过量的稀硝酸;氢氧化钠;(3)Ba(NO3)2、HCl、NaCl.

【题目】生活中处处有化学。从A或B中任选一个作答,若均作答,按A计分。
A | B |
(1)蒸馒头时,在发酵的面团中加入纯碱能中和酸味,纯碱的化学式为_______。 (2)干冰易升华,可用于_______。 | (1)生石灰常用作食品干燥剂,生石灰的化学式为__________。 (2)氢氧化钠易潮解,可用于__________。 |