题目内容
【题目】将一小块干冰放进一塑料袋,将口袋扎紧,一段时间后,塑料袋鼓起如图。
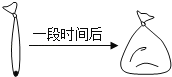
(1)从物质分类看,干冰属于_____(填“单质”或“化合物”)
(2)从物质组成看,干冰由_____和_____组成。
(3)从物质变化看,塑料袋鼓起的过程中干冰发生了_____(填“物理变化”或“化学变化”)
(4)从微观角度分析,塑料袋鼓起的原因是_____。
(5)将塑料袋中的气体通入含有紫色石蕊试液的水中,原来呈紫色的溶液变成_____色,有关化学反应的符号表达式为_____。
【答案】化合物 碳元素 氧元素 物理变化 分子间空隙增大 红 CO2+H2O=H2CO3
【解析】
单质是由同种元素组成的纯净物,化合物由两种或两种以上的元素组成的纯净物。
(1)干冰是二氧化碳的固态,是由碳、氧两种元素组成的纯净物,属于化合物。
(2)干冰是二氧化碳的固体形态,它是由碳元素、氧素组成的。
(3)塑料袋鼓起,是由于干冰由固态变成了气态的二氧化碳,只是状态发生了变化,没有新物质生成,属于物理变化。
(4)从分子的角度分析,塑料袋鼓起的原因是,分子间存在间隙,二氧化碳由固态变为气态时,分子间空隙增大。
(5)由于二氧化碳能与水化合生成了碳酸,碳酸显酸性,将塑料袋中的气体通入含有紫色石蕊试液的水中,原来呈紫色的溶液变成红色,有关化学反应的符号表达式为:
![]() 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目