题目内容
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 级别 | 一级指标 | 二级指标 | 三级指标 |
| 浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
(1)将含碘(I2)1.27mg的碘溶液加入到试管中;
(2)向试管内滴加2~3滴淀粉溶液,溶液显蓝色(淀粉遇I2便蓝)
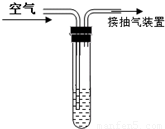
(3)通过抽气装置抽气,使空气由导气管进入试管与碘溶液接触.
(4)当溶液由蓝色变为无色时,测定通过空气的总量为1m3请你通过计算判断,该地区空气中二氧化硫的浓度级别.
【答案】分析:根据反应的化学方程式,由恰好完全反应消耗碘的质量计算出1m3空气中所含二氧化硫的质量,转化为标准表示法mg/m3,与级别标准对比,判断出空气中二氧化硫的浓度级别.
解答:解:设1m3的空气中含有二氧化硫的质量为x
SO2 +I2 +2H2O=H2SO4 +2HI
64 254
x 1.27mg
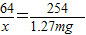
x=0.32mg
此空气中二氧化硫的最高浓度0.32mg/m3
因为0.15mg/m3<0.32mg/m3<0.50 mg/m3
所以该地区空气中二氧化硫的浓度级别为二级.
答:该地区空气中二氧化硫的浓度级别为二级
点评:本题为根据化学方程式的基本计算,在最后与级别标准对比时要注意:根据化学方程式计算所得值为空气中二氧化硫的质量,还需要转换成标准值.
解答:解:设1m3的空气中含有二氧化硫的质量为x
SO2 +I2 +2H2O=H2SO4 +2HI
64 254
x 1.27mg
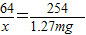
x=0.32mg
此空气中二氧化硫的最高浓度0.32mg/m3
因为0.15mg/m3<0.32mg/m3<0.50 mg/m3
所以该地区空气中二氧化硫的浓度级别为二级.
答:该地区空气中二氧化硫的浓度级别为二级
点评:本题为根据化学方程式的基本计算,在最后与级别标准对比时要注意:根据化学方程式计算所得值为空气中二氧化硫的质量,还需要转换成标准值.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
 二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如表所示:
二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如表所示:| 浓度限值(mg/m3) |
| 一级标准 二级标准 三级标准 0.15 0.50 0.70 |
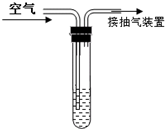 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
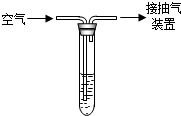
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示: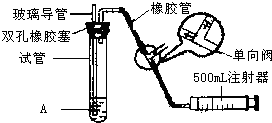 二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.
二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.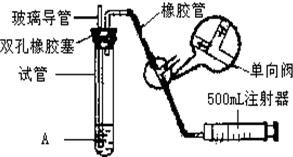 二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.
二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.