题目内容
燃烧法是一种常用于确定有机物元素组成的实验方法.请完成以下问题: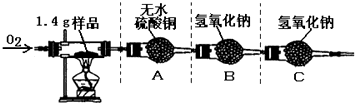
定性实验:
(1)甲烷的化学式是________.
(2)请写出通过甲烷燃烧确定其组成元素的实验方法:________
定量实验:
某有机食品保鲜袋除含有碳元素和氢元素外,可能含有氧元素.为确定该保鲜袋是否含有氧元素,进行如下实验探究.
实验过程:
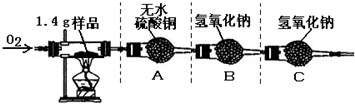
①按图示连接好仪器并检验该装置气密性
②称取1.4g该保鲜袋样品,剪碎后放在硬质玻璃试管中.
③用天平称得装置A的质量为82.0g;装置B的质量为85.0g
④持续通入纯O2,点燃酒精灯,直至保鲜袋样品完全燃烧
⑤实验结束,待冷却后,再次用天平称得装置A的质量为83.8g,装置B的质量为89.4g
请回答:
(1)查得资料:白色的无水硫酸铜易吸水,吸水后呈蓝色.根据实验后装置A中固体变蓝的现象说明该保鲜袋含有________元素.
(2)根据质量守恒定律,装置B在反应后增加的质量等于1.4g样品完全燃烧后生成的________(填化学式)的质量.
(3)通过计算可得,样品中碳元素的质量为________;氢元素的质量为________.
(4)结论:该保鲜袋样品________(填“含有”或“不含有”)氧元素.
(5)若无装置C,则实验测得样品中碳元素的质量会________(填“偏大”“偏小”或“无影响”)
解:【定性实验】(1)一个甲烷分子是由一个碳原子和四个氢原子构成的,故答案为:CH4
(2)故答案为:将甲烷点燃,在火焰上方罩一个冷而干燥的烧杯,一会儿,烧杯上有水珠出现,证明甲烷含有氢元素;迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,发现变浑浊,证明甲烷中含有碳元素.(或其他合理答案)
【定量实验】(1)白色的无水硫酸铜是检验有水生成,并吸收水的,吸水后呈蓝色,说明一定有氢元素;故答案为:氢(或H)
(2)氢氧化钠是吸收二氧化碳的,增加的质量就是二氧化碳的质量;故答案为:CO2
(3)样品中碳元素的质量=(89.4g-85.0g)×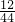 =1.2g,氢元素的质量=(83.8g-82.0g)×
=1.2g,氢元素的质量=(83.8g-82.0g)×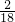 =0.2g;故答案为:1.2 g;0.2 g
=0.2g;故答案为:1.2 g;0.2 g
(4)根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;故答案为:不含有
(5)装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.故答案为:偏大
分析:一个甲烷分子是由一个碳原子和四个氢原子构成的;确定甲烷组成元素的实验方法是:将甲烷点燃,在火焰上方罩一个冷而干燥的烧杯,一会儿,烧杯上有水珠出现,证明甲烷含有氢元素;迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,发现变浑浊,证明甲烷中含有碳元素;白色的无水硫酸铜是检验有水生成,并吸收水的,吸水后呈蓝色,说明一定有氢元素;氢氧化钠是吸收二氧化碳的,增加的质量就是二氧化碳的质量;样品中碳元素的质量=(89.4g-85.0g)×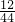 =1.2g,氢元素的质量=(83.8g-82.0g)×
=1.2g,氢元素的质量=(83.8g-82.0g)×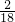 =0.2g;根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.
=0.2g;根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.
点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便;有关的计算要准确.
(2)故答案为:将甲烷点燃,在火焰上方罩一个冷而干燥的烧杯,一会儿,烧杯上有水珠出现,证明甲烷含有氢元素;迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,发现变浑浊,证明甲烷中含有碳元素.(或其他合理答案)
【定量实验】(1)白色的无水硫酸铜是检验有水生成,并吸收水的,吸水后呈蓝色,说明一定有氢元素;故答案为:氢(或H)
(2)氢氧化钠是吸收二氧化碳的,增加的质量就是二氧化碳的质量;故答案为:CO2
(3)样品中碳元素的质量=(89.4g-85.0g)×
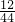 =1.2g,氢元素的质量=(83.8g-82.0g)×
=1.2g,氢元素的质量=(83.8g-82.0g)×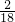 =0.2g;故答案为:1.2 g;0.2 g
=0.2g;故答案为:1.2 g;0.2 g(4)根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;故答案为:不含有
(5)装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.故答案为:偏大
分析:一个甲烷分子是由一个碳原子和四个氢原子构成的;确定甲烷组成元素的实验方法是:将甲烷点燃,在火焰上方罩一个冷而干燥的烧杯,一会儿,烧杯上有水珠出现,证明甲烷含有氢元素;迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,发现变浑浊,证明甲烷中含有碳元素;白色的无水硫酸铜是检验有水生成,并吸收水的,吸水后呈蓝色,说明一定有氢元素;氢氧化钠是吸收二氧化碳的,增加的质量就是二氧化碳的质量;样品中碳元素的质量=(89.4g-85.0g)×
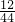 =1.2g,氢元素的质量=(83.8g-82.0g)×
=1.2g,氢元素的质量=(83.8g-82.0g)×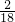 =0.2g;根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.
=0.2g;根据1.2g+0.2g=1.4g,因此该保鲜袋样品不含氧元素;装置C是吸收空气中的二氧化碳的,若无装置C,则实验测得样品中碳元素的质量会偏大.点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便;有关的计算要准确.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目