题目内容
【题目】向一定质量、一定溶质质量分数的稀盐酸中逐滴加入某碳酸钠溶液,实验过程中,产生气体质量与加入碳酸钠溶液的质量关系如图所示,试计算:
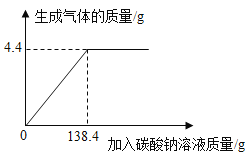
(1)恰好完全反应时,生成气体的质量为 g;
(2)恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量是多少?
(3)若恰好完全反应时所得溶液的溶质质量分数为5%,则稀盐酸的溶质质量分数是多少?
【答案】(1)4.4 (2)10.6g (3)7.3%
【解析】
试题分析:
(1)恰好完全反应时生成CO2的质量为4.4g;
(2)设恰好完全反应时,所加碳酸钠溶液中Na2CO3的质量为x,碳酸钠完全反应生成氯化钠的质量为y,消耗稀盐酸的溶质质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
![]()
x=10.6g
![]()
z=7.3g
y=11.7g
若恰好完全反应时所得溶液的质量=![]() =234g
=234g
稀盐酸的溶夜质量=234g+4.4g﹣138.4g=100g
则稀盐酸的溶质质量分数是![]() 100%=7.3%。
100%=7.3%。

练习册系列答案
相关题目