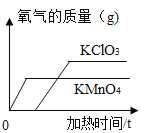
题目内容
【题目】实验室现有高锰酸钾、稀盐酸、石灰石、过氧化氧溶液及以下仪器:
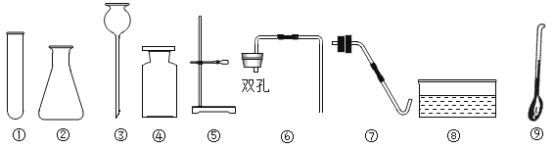
请回答下列问题:
(1)若利用上述药品和仪器制取氧气的整个实验过程中,需要用到的仪器有_______________________________,(填序号)还需要补充的仪器是__________,用品是棉花。制取该气体反应的化学方程式为_______________________。
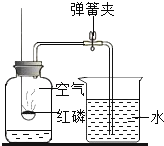
(2)①若利用上述药品和仪器制取二氧化碳,则仪器a在此实验中的作用是_________________;
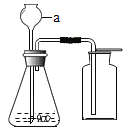
②实验过程中,气体能导出的原因是,因为______________(写出反应的化学方程式)使锥形瓶内气体______,气压变____________,在压强差作用下,气体从导管口逸出。
【答案】①④⑤⑦⑧⑨ 酒精灯 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 随时添加液体 CaCO3+2HCl=CaCl2+H2O+CO2↑ 质量增大 变大
K2MnO4 + MnO2 + O2↑ 随时添加液体 CaCO3+2HCl=CaCl2+H2O+CO2↑ 质量增大 变大
【解析】
(1)题干提供的药品没有二氧化锰,因此只能通过加热高锰酸钾制取氧气,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。若利用上述药品和仪器制取氧气,整个实验过程中,需要用到的仪器有①④⑤⑦⑧⑨;若用高锰酸钾制氧气还需要补充的仪器是酒精灯,用品是棉花;高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应的化学方程式为2KMnO4![]() K2MnO4 + MnO2 + O2↑;
K2MnO4 + MnO2 + O2↑;
(2)①若利用上述药品和仪器制取二氧化碳,则仪器a在此实验中的作用是随时添加液体;
②碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;碳酸钙与盐酸的反应使锥形瓶内气体质量增大,气压变大,在压强差作用下,气体从导管口逸出。

【题目】某化学学习小组为了测定某石灰石中碳酸钙的质量分数,取一定量的石灰石样品于烧杯中,加入适量的稀盐酸,恰好完全反应。有关数据记录如下表所示: (样品中其他成分 均不与稀盐酸反应且不溶于水)
反应前 | 反应后 | ||
实验数据 | 石灰石样品的质量 | 加入稀盐酸的质量 | 烧杯中剩余物质的总质量 |
32g | 60g | 83.2g | |
请计算: (1) 完全反应时生成气体的质量为_____ g.
(2) 该石灰石样品中碳酸钙的质量分数? _____(计算题中也会要用到化学力程式啊。看来,化学方程式非掌握不可。此刻,希望你能“破涕为笑”,愉快地结束本堂考试,祝你好运! )