题目内容
回答下列问题:
(1)实验室配制100g 10%的氯化钠溶液时,需要
①称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是下图的
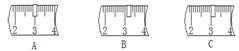
②下列仪器中,量取水时需要用
到d和
a.烧杯、b.10mL量筒、c.100mL量筒、d.滴管、e.玻璃棒、f.药匙、g.蒸发皿.
③为加快食盐的溶解速度,可以采用的方法有:
如果配制的溶液的溶质质量分数低于10%,你认为可能原因是
(2)在粗盐提纯中,将氯化钠溶液蒸发至有较多量固体析出后,应
(1)实验室配制100g 10%的氯化钠溶液时,需要
10
10
氯化钠固体.称量样品时,应把样品放在托盘天平的
左
左
盘里.①称量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是下图的
B
B
(填字母).
②下列仪器中,量取水时需要用
到d和
c
c
仪器(填序号),溶解时需要用到e和
a
a
仪器(填序号).(每空1分)a.烧杯、b.10mL量筒、c.100mL量筒、d.滴管、e.玻璃棒、f.药匙、g.蒸发皿.
③为加快食盐的溶解速度,可以采用的方法有:
将食盐研磨,加热或搅拌
将食盐研磨,加热或搅拌
如果配制的溶液的溶质质量分数低于10%,你认为可能原因是
量取水时仰视刻度量取
量取水时仰视刻度量取
.(任写一个).(2)在粗盐提纯中,将氯化钠溶液蒸发至有较多量固体析出后,应
停止加热(或熄灭酒精灯)
停止加热(或熄灭酒精灯)
,并用玻璃棒不断搅拌
并用玻璃棒不断搅拌
,利用余热将余下溶液蒸发至干.分析:该题要求学生:①要会运用溶质质量分数的公式计算溶质的质量,知道用托盘天平称量时要左物右码,游码的左端要对准所需的刻度.②溶解时要用到烧杯、玻璃棒等仪器,量取水时要根据情况选择量筒.③加快固体溶解所常用的方法有;搅拌、加热.④会分析配制溶液的溶质质量分数偏低的原因.
解答:解:(1)需要氯化钠的质量为:100克×10%=10克 称量时要左物右码.
故答案为:10,左.
①中游码对应的刻度应为3.1克,并且应该是游码的左端对准标尺的3.1克处.故答案为:B.
②该实验需水的质量为90ml所以量水时要用100ml的量筒,溶解时要用烧杯和玻璃棒.故答案为:c,a.
③为了加速食盐的溶解速度我们可以采用加热、用玻璃棒搅拌、把食盐研磨等方法.配制的质量分数偏低的原因有;取的溶剂水偏多,食盐偏少.当量取水时仰视刻度量取的水便会偏多,还有配制溶液的烧杯用少量的水润洗.当氯化钠晶体不纯,或者称量时左码右物,都会取的食盐偏少.故答案为:将食盐研磨,加热或搅拌.量取水时仰视刻度量取.
(2)在粗盐提纯中,为了防止液体飞溅要用玻璃棒不断的搅拌,当氯化钠溶液蒸发至有较多量固体析出后,应停止加热或熄灭酒精灯.故答案为:停止加热或熄灭酒精灯,并用玻璃棒不断搅拌.
故答案为:10,左.
①中游码对应的刻度应为3.1克,并且应该是游码的左端对准标尺的3.1克处.故答案为:B.
②该实验需水的质量为90ml所以量水时要用100ml的量筒,溶解时要用烧杯和玻璃棒.故答案为:c,a.
③为了加速食盐的溶解速度我们可以采用加热、用玻璃棒搅拌、把食盐研磨等方法.配制的质量分数偏低的原因有;取的溶剂水偏多,食盐偏少.当量取水时仰视刻度量取的水便会偏多,还有配制溶液的烧杯用少量的水润洗.当氯化钠晶体不纯,或者称量时左码右物,都会取的食盐偏少.故答案为:将食盐研磨,加热或搅拌.量取水时仰视刻度量取.
(2)在粗盐提纯中,为了防止液体飞溅要用玻璃棒不断的搅拌,当氯化钠溶液蒸发至有较多量固体析出后,应停止加热或熄灭酒精灯.故答案为:停止加热或熄灭酒精灯,并用玻璃棒不断搅拌.
点评:本题考查的内容不少,但是都是围绕着配制一定质量一定质量分数的溶液的步骤展开的,要求学生对该类题型要动脑思考,且加以总结.为以后的考试打下良好的基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件.为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:
认真分析数据,回答下列问题:
(1)黄铜中铜的质量分数为
(2)恰好完全反应时,溶液中溶质的质量分数是.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)黄铜中铜的质量分数为
(2)恰好完全反应时,溶液中溶质的质量分数是.
溶液与人类的生活息息相关,溶液的配制是日常生活和化学实验中的常见操作.下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃).
请仔细分析后回答下列问题:
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐 (填增大、减不或不变);氨水的密度逐渐 (填增大、减小或不变)
(2)取12%的硫酸溶液100g配制成6%的溶液,向100g12%的硫酸溶液中加水的质量
应 100g(填大于、小于或等于).
(3)向100g24%的氨水中加入100g水,摇匀,溶液体积是 mL(保留到0.1).
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/mL | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/mL | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐
(2)取12%的硫酸溶液100g配制成6%的溶液,向100g12%的硫酸溶液中加水的质量
应
(3)向100g24%的氨水中加入100g水,摇匀,溶液体积是
